Dựa vào tương tác van der Waals, hãy giải thích tại sao đơn chất N2 khó hoá lỏng và ít tan trong nước.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

So sánh được tính chất vật lí giữa các phân tử dựa vào liên kết hydrogen và tương tác van der Waals.

Để so sánh được tính chất vật lí giữa các phân tử, chúng ta cần nắm được những ý sau:
- Liên kết hydrogen được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron hóa trị chưa tham gia liên kết.
⇒ Liên kết hydrogen làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của nước.
- Tương tác van der Waals là tương tác tĩnh điện lưỡng cực – lưỡng cực được hình thành giữa các phân tử hay nguyên tử.
⇒ Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất.

Lực Van der Waals là một loại tương tác giữa các phần tử có tiếp xúc với nhau, được đặt tên của nhà vật lý người Hà Lan Johannes Diderik van der Waals, mô tả một loại tương tác phụ thuộc vào khoảng cách giữa các phần tử, công bố đầu tiên vào năm 1873. Các phần tử tham gia vào lực này thường là phân tử.
Thực chất, lực Van der Waals là lực tĩnh điện, thường xuất hiện giữa các phân tử chất khí, khí hóa lỏng hoặc hóa rắn, và trong hầu hết các chất lỏng và chất rắn hữu cơ.
- Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất. Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng.
-Tương tác van der Waals làm tăng nhiệt độ sôi và nhiệt độ nóng chảy. ⟹ Khí hiếm có nhiệt độ nóng chảy thấp nhất là He và cao nhất là Xe.

Các hiện tượng có xuất hiện của liên kết hydrogen, tương tác van der Waals trong thực tiễn:
- Liên kết hydrogen: có trong DNA để tạo thành các chuỗi kép, hình thành cấu trúc chuỗi cấp trong các protein…
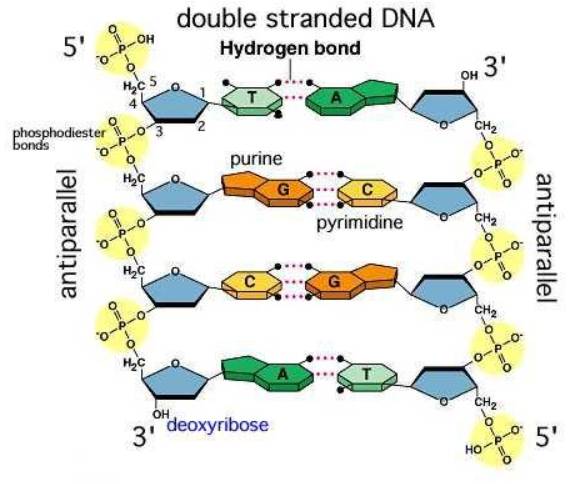
Liên kết hydrogen trong nước giúp duy trì sự ổn định chất lỏng trong một phạm vi diện rộng, làm cho băng đá nhẹ hơn nước lỏng bởi vậy băng nổi trên mặt nước, nước có thể bay hơi làm cho hệ sinh thái trên Trái Đất tuần hoàn tự nhiên.
- Lực tương tác van der Waals: sự bám hút của hạt bụi trên bề măt; tắc kè, thạch sùng có thể bám chắc trên các bề mặt trơn nhẵn; khả năng kết dính của băng dính; sự hấp phụ chất độc và phân tử màu trong nước bởi than hoạt tính…

Trong tinh thể sulfur, các phân tử S8 tương tác với nhau bằng lực van der Waals yếu do đó đơn chất sulfur có nhiệt độ nóng chảy thấp, sulfur nóng chảy ở nhiệt độ 113oC.

a, - Hiện tượng: Sau khi cho nước vào thấy có hơi màu tím thoát ra.
- Giải thích: Sau khi thêm nước, phản ứng giữa Al và I2 xảy ra, tỏa nhiệt mạnh là I2 thăng hoa.
b, PT: \(2Al+3I_2\underrightarrow{^{H_2O}}2AlI_3\)
Vai trò chất tham gia: Al là chất khử, I2 là chất oxy hóa, H2O là xúc tác.
c, - Do iot có độ âm điện nhỏ, bán kính nguyên tử lớn nên COI2 kém bền → không tồn tại.

a. Giải thích tại sao khi cho muối ăn vào cốc nước lạnh thì muối ăn tan ít,
khi cho muối ăn vào cốc nước nóng thì muối ăn tan nhiều hơn?
=> đó là theo nguyên lí độ tan của dung môi
b. Hãy giải thích tại sao muốn bảo quản tốt các loại nước có ga ta phải
đậy kín nắp lọ và bảo quản lọ nước đó trong tủ lạnh.
=> tránh làm nổ bình do áp suất tăng lên do thể tích bình giảm xuống sẽ gây nổ
c. Giải thích tại sao khi cho đường vào cốc nước lạnh thì đường tan ít,
khi cho đường vào cốc nước nóng thì đường tan nhiều .
do các nguyên tử nước nếu lành thì ít hoiatj động , nước co lại khiến các phân tử đường ko vào đc , nếu nc nóng thì ngược lại
d. Hãy giải thích tại sao khi mở bình nước ngọt có ga lại có nhiều bọt khí thoát ra ?
đó là phản ứng của axit và goocsHCO3 trong bình nước ngọt đó

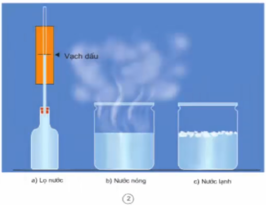
- Khi đặt vào nước nóng nước trong lọ nở ra (nước cao hơn vạch dấu).
- Khi đặt vào nước lạnh nước trong lọ co lại (thấp hơn vạch dấu).
- Vì nước và các chất lỏng nở ra khi nóng lên và co lại khi lạnh đi nên khi nhiệt độ thay đổi mức chất lỏng trong ống nhiệt kế cũng thay đổi theo.
Vì nitrogen có nhiều electron nên tương tác London tăng, nhiệt độ nóng chảy, nhiệt độ sôi tăng. Vậy nên đơn chất N2 khó hoá lỏng và ít tan trong nước (không phân cực).