Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Các hiện tượng có xuất hiện của liên kết hydrogen, tương tác van der Waals trong thực tiễn:
- Liên kết hydrogen: có trong DNA để tạo thành các chuỗi kép, hình thành cấu trúc chuỗi cấp trong các protein…
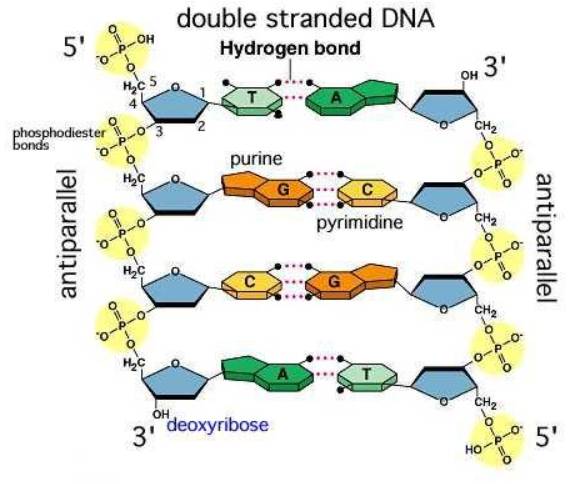
Liên kết hydrogen trong nước giúp duy trì sự ổn định chất lỏng trong một phạm vi diện rộng, làm cho băng đá nhẹ hơn nước lỏng bởi vậy băng nổi trên mặt nước, nước có thể bay hơi làm cho hệ sinh thái trên Trái Đất tuần hoàn tự nhiên.
- Lực tương tác van der Waals: sự bám hút của hạt bụi trên bề măt; tắc kè, thạch sùng có thể bám chắc trên các bề mặt trơn nhẵn; khả năng kết dính của băng dính; sự hấp phụ chất độc và phân tử màu trong nước bởi than hoạt tính…

Lực Van der Waals là một loại tương tác giữa các phần tử có tiếp xúc với nhau, được đặt tên của nhà vật lý người Hà Lan Johannes Diderik van der Waals, mô tả một loại tương tác phụ thuộc vào khoảng cách giữa các phần tử, công bố đầu tiên vào năm 1873. Các phần tử tham gia vào lực này thường là phân tử.
Thực chất, lực Van der Waals là lực tĩnh điện, thường xuất hiện giữa các phân tử chất khí, khí hóa lỏng hoặc hóa rắn, và trong hầu hết các chất lỏng và chất rắn hữu cơ.
- Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất. Khi khối lượng phân tử tăng, kích thước phân tử tăng thì tương tác van der Waals tăng.
-Tương tác van der Waals làm tăng nhiệt độ sôi và nhiệt độ nóng chảy. ⟹ Khí hiếm có nhiệt độ nóng chảy thấp nhất là He và cao nhất là Xe.

- CT electron và CT Lewis của NH3:
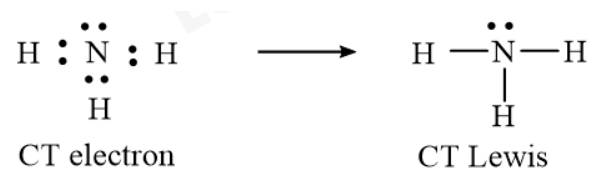
⟹ NH3 còn 1 cặp electron riêng của N.
- Vì N còn 1 của phân tử NH3 còn 1 cặp electron riêng và có độ âm điện lớn hơn nguyên tử H của phân tử H2O.
⟹ Một phân tử H2O có khả năng tạo thành liên kết hydrogen với một phân tử NH3, liên kết tạo bởi H và N.

Đáp án D
Trong HClO: H-O-Cl có liên kết H-O là cộng hoá trị phân cực (Dc = 1,4)
liên kết O-Cl là cộng hoá trị phân cực yếu (Dc = 0,5)
Trong KHS: K-S-H có liên kết K-S là liên kết ion (Dc = 1,7)
liên kết S-H là cộng hoá trị phân cực yếu (Dc = 0,4)

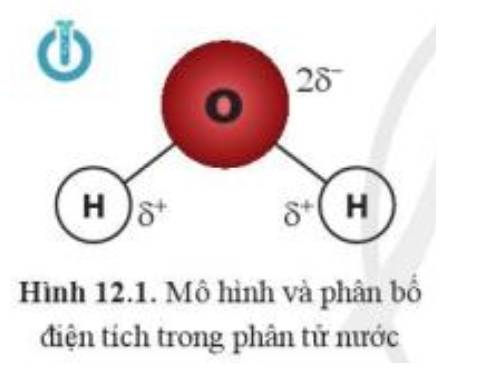
Dựa vào sự phân bố điện tích trong phân tử nước (hình 12.1), liên kết giữa hai phân tử nước được hình thành qua cặp nguyên tử O với H.
Do nguyên tử H mang điện tích dương nên liên kết với nguyên tử mang điện tích âm là O. Ngoài ra O còn 2 cặp electron riêng và độ âm điện lớn hơn H. Vì vậy phân tử H2O được tạo bởi các liên kết hydrogen của cặp nguyên tử O – H, liên kết này có bản chất tĩnh điện, tương tác hút điện giữa và , giúp liên kết hai phân tử H2O với nhau.

Na --> Na+ + 1e
S + 2e --> S2-
2 ion Na+ và S2- trái dấu nên hút nhau bởi lực hút tĩnh điện
2Na+ + S2- --> Na2S
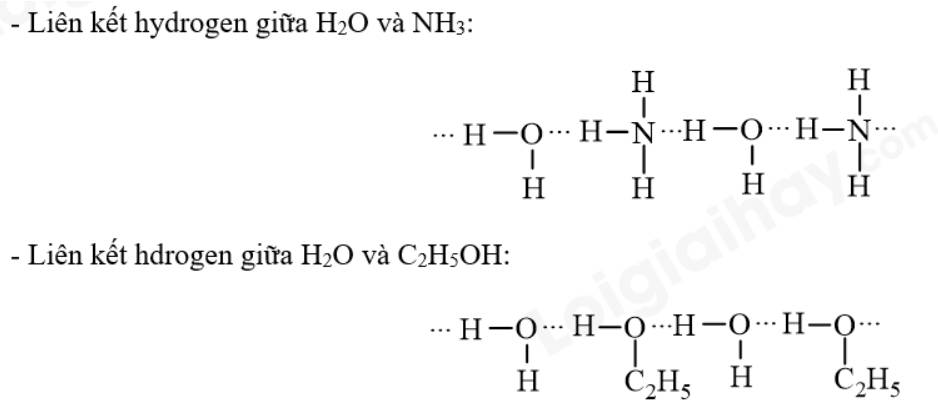
Để so sánh được tính chất vật lí giữa các phân tử, chúng ta cần nắm được những ý sau:
- Liên kết hydrogen được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron hóa trị chưa tham gia liên kết.
⇒ Liên kết hydrogen làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của nước.
- Tương tác van der Waals là tương tác tĩnh điện lưỡng cực – lưỡng cực được hình thành giữa các phân tử hay nguyên tử.
⇒ Tương tác van der Waals làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của các chất.