Tính số mol của 22g hỗn hợp Al và Fe
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH: 2Al + 6HCl -> 2AlCl3 + 3H2
Fe + 2HCl -> FeCl2 + H2
Giả sử hh chỉ gồm Fe
nFe = \(\dfrac{22}{56}\approx0,4\left(mol\right)\)
Ta có tỉ lệ : \(\dfrac{n_{Fe}}{1}=0,4\) > \(\dfrac{n_{HCl}}{2}=\dfrac{0,6}{2}=0,3\)
=>Fe dư, HCl hết
hay hh ko tan hết

Gọi số mol của Al và Fe lần lượt là x và y
Vì số mol của Al gấp 2 lần Fe nên x=2y (1)
Và khối lượng của Fe và Al là 11g nên
27x+56y=12 (2)
Giải HPT: \(\left\{{}\begin{matrix}\text{27x+56y=12 }\\\text{x=2y }\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}\text{x=0,2 mol}\\\text{y=0,1 mol}\end{matrix}\right.\)
\(\rightarrow\)mAl=27.0,2=5,4
mAl=56.0,1=5,6

Ta có:
\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{Al}=\dfrac{3,24}{27}=0,12\left(mol\right)\)
Nên số mol của hỗn hợp X là:
\(n_X=n_{Fe}+n_{Al}=0,2+0,12=0,32\left(mol\right)\)

- Gọi số mol Al và Fe trong hốn hợp lần lượt là a, b mol
PTKL : 27a + 56b = 22
BTe : 3a + 3b = 1,8
=> a = 0,4 và b = 0,2 .
=> mAl = 10,8g và mFe = 11,2 g
b, Sau phản ứng thu được muối Al2(SO4)3 và Fe2(SO4)3 .
=> mM = 108,4g
\(n_{Al}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(\Rightarrow27a+56b=22\left(1\right)\)
\(n_{SO_2}=\dfrac{20.16}{22.4}=0.9\left(mol\right)\)
\(2Fe+6H_2SO_{4\left(đ\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
\(2Al+6H_2SO_{4\left(đ\right)}\rightarrow Al_2\left(SO_4\right)_3+3SO_2+6H_2O\)
\(n_{SO_2}=1.5a+1.5b=0.9\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.4,b=0.2\)
\(m_{Al}=0.4\cdot27=10.8\left(g\right)\)
\(m_{Fe}=11.2\left(g\right)\)
\(m_{Muối}=0.2\cdot342+0.1\cdot400=108.4\left(g\right)\)

Gọi : \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\)⇒ 56x + 27y = 13,7(1)
\(Fe + 2HCl \to FeCl_2 + H_2\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\)
Theo PTHH :
\(n_{H_2} = x + 1,5y = \dfrac{24,64}{22,4} = 1,1(2)\)
Từ (1)(2) suy ra : x = -0,16<0
(Sai đề)

F22: Tính số mol mỗi kim loại ? Biết :
a. 9,96 gam hỗn hợp X ( Fe , Al có tỷ lệ mol 1 : 1) .
Gọi x, y lần lượt là số mol Fe, Al
\(\left\{{}\begin{matrix}56x+27y=9,96\\x=y\end{matrix}\right.\)
=> x=y= 0,12(mol)
b. 27,6 gam hỗn hợp Y ( Fe , Cu có tỷ lệ mol 1 : 2) .
Gọi x, y lần lượt là số mol Fe, Cu
\(\left\{{}\begin{matrix}56x+64y=27,6\\\dfrac{x}{y}=\dfrac{1}{2}\end{matrix}\right.\)
=> x= 0,15; y=0,3
c. 29,52 gam hỗn hợp Z ( Cu, Al có tỷ lệ mol 3 : 2 ) .
Gọi x, y lần lượt là số mol Cu, Al
\(\left\{{}\begin{matrix}64x+27y=29,52\\\dfrac{x}{y}=\dfrac{3}{2}\end{matrix}\right.\)
=> x= 0,36 ; y=0,24
F23: 11 gam hỗn hợp X (Al, Fe) có tổng số mol là 0,3. Tính khối lượng mỗi kim loại ?
Gọi x, y lần lượt là số mol Al, Fe
\(\left\{{}\begin{matrix}27x+56y=11\\x+y=0,3\end{matrix}\right.\)
=> x=0,2 , y =0,1
=> \(\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Fe}=0,1.56=5,6\left(g\right)\end{matrix}\right.\)

a)
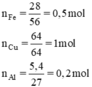
b) VCO2 = 22,4 .0,175 = 3,92l.
VH2 = 22,4 .1,25 = 28l.
VN2 = 22,4.3 = 67,2l.
c) Số mol của hỗn hợp khí bằng tổng số mol của từng khí.
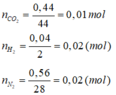
nhh = nCO2 + nH2 + nN2 = 0,01 + 0,02 + 0,02 = 0,05 mol
Vhh khí = (0,01 + 0,02 + 0,02) . 22,4 = 1,12l.

a.
\(V_{H_2S}=0.75\cdot22.4=16.8\left(l\right)\)
\(V_{SO_2}=\dfrac{12.8}{64}\cdot22.4=4.48\left(l\right)\)
\(V_{O_2}=\dfrac{3.2}{32}\cdot22.4=2.24\left(l\right)\)
b.
\(n_{hh}=\dfrac{22}{44}+\dfrac{3.55}{71}+\dfrac{0.14}{28}=0.555\left(mol\right)\)
\(V_{hh}=0.555\cdot22.4=12.432\left(l\right)\)

tau cũng định hỏi câu này
Lập CTHH ( bạn tự lập , dựa vào hóa trị của Al và Fe nhé =)) )
Sau khi lập ta được : CTHH Al2Fe3
Theo bài ra ta có :
Khối lượng mol của Al2Fe3 là :
\(M_{Al_2Fe_3}=\left(27\times2\right)+\left(56\times3\right)=222\)(g/mol)
Số mol của Al2Fe3 là :
\(n_{Al_2Fe_3}=\frac{m_{Al_2Fe_3}}{M_{Al_2Fe_3}}=\frac{22}{222}=\frac{11}{111}\approx0,01\left(mol\right)\)
Vậy số mol của Al2Fe3 là 0,01 (mol)
Chúc bạn học tốt =))