Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Gọi số hạt proton, notron, electron của R là Z, N và Z.
Theo giả thiết đề bài ta có hệ: 2 Z + N = 34 N - Z = 1 ⇔ Z = 11 N = 12
Khi đó R có cấu hình electron là 1s22s22p63s1.
Do đó số electron độc thân của R là 1.

\(\left\{{}\begin{matrix}P+N+E=34\\P=E\\N-E=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2E+N=34\\N-E=1\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=11\\N=12\end{matrix}\right.\\ a.A_R=Z_R+N_R=11+12=23\left(đ.v.C\right)\\ b.KH:^{23}_{11}Na\)

Vì trong nguyên tử số hạt electron bằng số hạt proton nên trong R có số hạt proton, notron và electron lần lượt là Z, N và Z.
Theo giả thiết đề bài ta có:
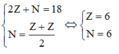
Khi đó cấu hình electron của R là 1s22s22p2.
Do đó số electron độc thân của R là 4.
Đáp án D

Đáp án D
Vì trong nguyên tử số hạt electron bằng số hạt proton nên trong R có số hạt proton, notron và electron lần lượt là Z, N và Z.
Theo giả thiết đề bài ta có: 2 Z + N = 18 N = Z + Z 2 ⇔ Z = 6 N = 6
Khi đó cấu hình electron của R là 1s22s22p2.
Do đó số electron độc thân của R là 4.

Đáp án B.
Tổng số các loại hạt proton, nơtron và electron của R là 18
p + n + e = 18 => 2p + n = 18 (1)
Số hạt không mang điện bằng trung bình cộng của tổng số hạt mang điện
n = (p+e)/2 hay n = p = e (2)
Từ (1), (2) ta có p = e = n =6
Cấu hình e của R : 1s2 2s2 2p2. Số electron độc thân = 2

\(\left\{{}\begin{matrix}p+e+n=18\\n=\frac{\left(p+e\right)}{2}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2p+n=18\\n=\frac{2p}{2}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2p+n=18\\n=p\end{matrix}\right.\Leftrightarrow p=e=n=6\)
\(\rightarrow R:C\left(Cacbon\right)\)
Cấu hình: \(1s^22s^22p^2\)
Chọn B
tổng hạt: 2p + n = 18 (1)
Tổng số hạt không mang điện bằng trung bình cộng tổng số hạt mang điện:
\(\Leftrightarrow n=\frac{2p}{2}\Leftrightarrow2n-2p=0\left(2\right)\)
Từ (1) và (2) ta có hpt:
\(\Rightarrow\left\{{}\begin{matrix}2p+n=18\\2n-2p=0\end{matrix}\right.\) \(\Leftrightarrow p=e=n=6\)
Vì p = 6 nên cấu hình của nguyên tử R là:
\(1s^22s^22p^2\)
Vậy số electron độc thân của R là 2 ( chọn câu b )
( giải thích thêm: Vì \(2s^2\) đã bão hòa )

1.\(\left\{{}\begin{matrix}Z+N=35\\N-Z=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}Z=17\left(Cl\right)\\N=18\end{matrix}\right.\)
A=Z+N=17+18=35
\(\Rightarrow^{35}_{17}Cl\)
2.\(\left\{{}\begin{matrix}2Z+N=115\\2Z-N=25\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}Z=35\left(Br\right)\\N=45\end{matrix}\right.\)
\(\Rightarrow A=35+45=80\)
\(\Rightarrow^{80}_{35}Br\)

ta co p+n+e =34
ma P=E suy ra 2p +n =34
2p =1,833 +n
p<n<1,5p
suy ra 3p<2p+n<3,5p
3p<34<3,5p
34:3,5<p<34:3
=9,7<p<11,3
thu p=10 va 11 ta thay 11 hop li nen chon p=11=e
r la na va la nguyen to kim loai vi co 1e lop ngoai cung

Bài 1:
Áp dụng biểu thức điều kiện bền :
\(\dfrac{S}{3,5}\le Z\le\dfrac{S}{3}\Leftrightarrow\dfrac{34}{3,5}\le Z\le\dfrac{34}{3}\Leftrightarrow9,7\le Z\le11,3\)
\(\Rightarrow Z=10,
11\)
Khi Z=10
\(1s^22s^22p^6\left(L\right)\)
Khi Z=11
\(1s^22s^22p^63s^1
\left(N\right)\)
\(\Rightarrow Z=11
\)
Nguyên tử này là : \(\begin{matrix}23\\11\end{matrix}Na\)
Bài 2:
Áp dụng biểu thức điều kiện bền :
\(\dfrac{S}{3,5}\le Z\le\dfrac{S}{3}\Leftrightarrow\dfrac{40}{3,5}\le Z\le\dfrac{40}{3}\Leftrightarrow11,4\le Z\le13,3\)
\(\Rightarrow Z=12,
13\)
Khi Z=12
\(1s^22s^22p^63s^2\left(L\right)\)
Khi Z=13
\(1s^22s^22p^63s^23p^1\left(N\right)\)
\(\Rightarrow Z=13\)
Vậy nguyên tử này là: \(\begin{matrix}27\\13\end{matrix}Al\)
Gọi số hạt proton, notron, electron của R là Z, N và Z.
Theo giả thiết đề bài ta có hệ:
Khi đó R có cấu hình electron là 1s22s22p63s1.
Do đó số electron độc thân của R là 1.
Đáp án D