Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khối lượng oxi thoát ra: m O 2 = 197 + 3 – 152 = 48(g)
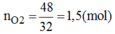
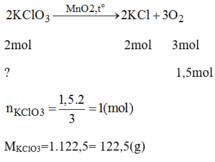
PTHH của phản ứng:
Khối lượng của KCl trong hỗn hợp ban đầu:
m K C l = 197-122,5 = 74,5(g)
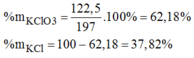

Gọi x, y lần lượt là số mol của KClO3 , KCl
Pt: \(2KClO_3\rightarrow2KCl+3O_2\)
x y
mKCl = 152 - 3 = 149 (g)
\(\Rightarrow\left\{{}\begin{matrix}122,5x+74,5y=197\\74,5x+74,5y=149\end{matrix}\right.\) \(\Rightarrow x=y=1\)
\(\%KClO_3=\dfrac{1.122,5}{197}.100=62,18\%\)
\(\%KCl=100-62,18=37,82\%\)

Sau phản ứng thu được: \(76-2=74gKCl\)
\(\Rightarrow n_{KCls.p.ứ}=\frac{74}{74,5}=1mol\)
Gọi \(x\) là mol \(KCl;y\) là mol \(KClO_3\) ban đầu.
\(\Rightarrow74,5x+122,5y=98\left(1\right)\)
\(PTHH:2KClO_3\overset{t^0}{\rightarrow}2KCl+3O_2\)
\(\Rightarrow n_{KCl.nung}=y\)
\(\Rightarrow x+y=1\left(2\right)\)
\(\left(1\right)\left(2\right)\Rightarrow x=y=0,5\)
\(m_{KCl}=0,5.74,5=37,25g\)
\(m_{KClO_3}=0,5.122,5=61,25g\)

a) 2KClO3------> 2KCl+ 3O2
công thức tính khối lượng:
m KClo3= m KCl+ m O2
b) m KCLo3= 14,9+9,6=24,5g

Gọi 2x, y lần lượt là số mol của KClO3, KCl
\(2KClO_3-t^0->2KCl+3O2\)
2x.............................2x...............3x
\(\left[{}\begin{matrix}74,5.\left(2x+y\right)=35,6-2\\74,5y+245x=48\end{matrix}\right.\)
\(\Leftrightarrow\left[{}\begin{matrix}x=0,15\\y=0,15\end{matrix}\right.\)
\(m_{KCl}=0,15.74,5=11,175\left(g\right)\)
\(m_{KClO_3}=0,15.2.122,5=36,75\left(g\right)\)
\(\%KCl_{tt}=\dfrac{0,15.2.74,5}{74,5}.100\%=46,5625\%\)
\(\%KCl=100\%-46,5625\%=53,4375\%\)
t k chăc lắm có j sai thì mn sửa hộ :)
Trộn đều 2g MnO2 và 98g hỗn hợp X gồm KClO3 và KCl rồi đun nóng đến khi phản ứng xảy ra hoàn toàn thì thu được chất rắn cân nặng 76g. Xác định khối lượng mỗi muối trong hỗn hợp X.
#giải #dùm #mình #với #gấp #lắm #ạ

pt: 2KClO3---MnO2/t*--->2KCl+3O2
mO2=197+3-152=48(g)
=>nO2=48/32=1,5(mol)
Theo pt: nKClO3=2/3nO2=2/3.1,5=1(mol)
=>mKClO3=1.122,5=122,5(g)
=>%mKClO3=122,5/197.100~62,18%
=>%mKCl=100%-62,18%=37,82%

Vì Mn02 là chất xúc tác cho nên chất rắn còn lại
gồm KCl và Mn02
=>mKCl=152-3=149(g)
Gọi x là số mol KCl03 ,y là số mol KCl tạo thành:
122.5x+74.5y=197 74.5x+74.5y=149
<=>x=y=1
=>mKCl03=1*122.5=122.5(g)
=>%KCl03=122.5*100%/197=62.18%
=>%KCl=100%-62.18%=37.82%
C2:Vì khối lượng còn lại giảm so với ban đầu do oxi thoát ra ngoài
=>m02=197+3-152=48(g)
=>n02=48/32=1.5mol
=>nKCl03=1.5*2/3=1mol
=>%KCl03=(1*122.5)*100%/197=62.18%
=>%KCl=100%-62.18%=37.82%

giúp mình trả lời nhanh câu hỏi trên nhé mình cần rất gấp ngay bây giờ .giúp mình tí nhá cám ơn cả nhà nhiều
Khối lượng oxi thoát ra là: \(197+3-152=48\left(g\right)\)
Số mol \(O_2=\dfrac{48}{3,2}=1,5\left(mol\right)\)
Phương trình hóa học của phản ứng:
\(2KCLO_3\xrightarrow[]{MnO_2,t^o}2KCL+3O_2\)
2 mol 3 mol
\(\dfrac{1,5.2}{3}=1\left(mol\right)\leftarrow1,5mol\)
Khối lượng \(KCLO_3\) trong hỗn hợp: \(1.122,5=122,5\left(g\right)\)
Khối lượng KCl trong hỗn hợp ban đầu: \(197-122,5=74,5\left(g\right)\)
\(\rightarrow\%m_{KCLO_2}=62,18\%;\%m_{KCL}=37,82\%2\)