Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chất rắn chứa 3 kim loại nên Fe dư
\(Al+3AgNO_3\rightarrow Al\left(NO_3\right)_3+3Ag\)
x/3_____ x_____________________
\(2Al+3Cu\left(NO_3\right)_2\rightarrow2Al\left(NO_3\right)_3+3Cu\)
\(\frac{0,03-x}{3}\rightarrow0,0045-0,5x\)
\(Fe+Cu\left(NO_3\right)_2\rightarrow Fe\left(NO_3\right)_2+Cu\)
1,5x-0,045__1,5x-0,045 __Fe còn dư = 0,095-1,5x
Ta có :
\(m_{kl}=x.108+\left(0,045-0,5x\right).64+\left(0,095-1,5x\right).56=8,12\)
\(\rightarrow x=0,01\)
\(\rightarrow CM=0,1M\)

Fe + Cu(NO3)2 \(\rightarrow\)Fe(NO3)2 + Cu (1)
Fe + 2AgNO3 \(\rightarrow\)Fe(NO3)2 + 2Ag (2)
nCu(NO3)2=0,1.0,5=0,05(mol)
nAgNO3=0,1.2=0,2(mol)
Theo PTHH 1 và 2 ta có:
nFe(1)=nCu=nCu(NO3)2=0,05(mol)
2nFe(2)=nAgNO3=nAg=0,2(mol)
nFe(2)=0,1(mol)
mFe tăng(1)=0,05.(64-56)=0,4(g)
mFe tăng(2)=108.0,2-56.0,1=16
Vaayh thanh Fe tăng 16+0,4=16,4g
đề nhầm kìa bạn
thả một thanh kim loại Fe rồi sau đó là lấy thanh chì ra là sao chắc là bạn ghi nhầm

\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\)
\(n_{Al}=\dfrac{0,81}{27}=0,03mol\)
\(B:8,12g\left\{{}\begin{matrix}Cu:a\left(mol\right)\\Ag:b\left(mol\right)\\Fe:c\left(mol\right)\end{matrix}\right.\Rightarrow64a+108b+56c=8,12\)(*)
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,03 0,03
\(\Rightarrow c=n_{Fe}=0,03mol\)
Thay vào (*) ta được: \(64a+108b=8,12-0,03\cdot56\left(1\right)\)
\(n_{Fepư}=0,05-0,03=0,02mol\)
\(BTe:2n_{Cu}+n_{Ag}=3n_{Fepư}+2n_{H_2}\)
\(\Rightarrow2a+b=2\cdot0,02+3\cdot0,03\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,03\end{matrix}\right.\)
\(C_{M_{Cu\left(NO_3\right)_2}}=\dfrac{0,05}{0,1}=0,5M\)
\(C_{M_{AgNO_3}}=\dfrac{0,03}{0,1}=0,3M\)

Câu 1:
2M+nCuSO4\(\rightarrow\)M2(SO4)n+nCu
2M+nFeSO4\(\rightarrow\)M2(SO4)n+nFe
- Gọi a là số mol của M
- Độ tăng khối lượng PTHH1:
64na/2-Ma=20 hay(32n-M).a=20
- Độ tăng khối lượng PTHH2:
56.na/2-Ma=16 hay (28n-M)a=16
Lập tỉ số ta được:\(\dfrac{32n-M}{28n-M}=\dfrac{20}{16}=1,25\)
32n-M=35n-1,25M hay 0,25M=3n hay M=12n
n=1\(\rightarrow\)M=12(loại)
n=2\(\rightarrow\)M=24(Mg)
n=3\(\rightarrow\)M=36(loại)
Câu 2:Gọi A là khối lượng thanh R ban đầu.
R+Cu(NO3)2\(\rightarrow\)R(NO3)2+Cu
R+Pb(NO3)2\(\rightarrow\)R(NO3)2+Pb
- Gọi số mol Cu(NO3)2 và Pb(NO3)2 là x mol
- Độ giảm thanh 1: \(\dfrac{\left(R-64\right)x}{A}.100=0,2\)
- Độ tăng thanh 2: \(\dfrac{\left(207-R\right)x}{A}.100=28,4\)
Lập tỉ số: \(\dfrac{207-R}{R-64}=\dfrac{28,4}{0,2}=142\)
207-R=142R-9088 hay 143R=9295 suy ra R=65(Zn)

$a)PTHH:Fe+2HCl\to FeCl_2+H_2$
$\Rightarrow n_{Fe}=n_{H_2}=\dfrac{2,479}{24,79}=0,1(mol)$
$\Rightarrow \%m_{Fe}=\dfrac{0,1.56}{12}.100\%=46,67\%$
$\Rightarrow \%m_{Cu}=100-46,67=53,33\%$
$b)n_{FeCl_2}=n_{Fe}=0,1(mol)$
$\Rightarrow m_{FeCl_2}=0,1.127=12,7(g)$
$c)n_{HCl}=2n_{Fe}=0,2(mol)$
$\Rightarrow C_{M_{HCl}}=\dfrac{0,2}{0,1}=2M$

Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
nAgNO3 = V1. 0,5 (mol)
=> nAg = 0,5.V1 mol và nFe dư = \(\dfrac{0,5.V_1}{2}\)(mol)
=> Khối lượng chất rắn thu được = mAg + mFe dư
= 108.0,5.V1 + m- \(\dfrac{56.0,5V_1}{2}\)= m+ 40V1 (gam)
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
nCu(NO3)2 = 0,2.V2 (mol)
Giả sử Fe dư , Cu(NO3)2 hết => nCu = nCu(NO3)2 =nFe phản ứng = 0,2.V2 (mol)
Khối lượng chất rắn sau phản ứng = mCu + mFe dư(mFe ban đầu - mFe phản ứng)
= 64.0,2.V2 + m - 56.0,2.V2 = 1,6V2 + m (gam)
Khối lượng chất rắn thu được ở 2 TN là như nhau
=> 1,6V2 + m = m + 40V1
<=> 1,6V2 = 40V1
<=> \(\dfrac{V_1}{V_2}\)= \(\dfrac{1,6}{40}\)=\(\dfrac{1}{25}\)

a) A chứa 3 muối là Mg(NO3)2, Al(NO3)3, NaNO3
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
B chứa các kim loại: Ag, Cu, Fe, Zn
b)
B chứa 4 kim loại: Ag, Cu, Fe, Zn
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
=> A chứa các muối: NaNO3, Mg(NO3)2, Al(NO3)3 và có thể có Zn(NO3)2
a) A chứa 3 muối là Mg(NO3)2, Al(NO3)3, NaNO3
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
\(3Mg+2Al\left(NO_3\right)_3\rightarrow3Mg\left(NO_3\right)_2+2Al\)
B chứa các kim loại: Ag, Cu, Fe, Zn và có thể có Al
b)
B chứa 4 kim loại: Ag, Cu, Fe, Zn
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
=> A chứa các muối: NaNO3, Mg(NO3)2, Al(NO3)3 và có thể có Zn(NO3)2

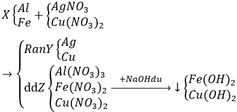
Pt:
Al + 3AgNO3 → Al(NO3)3 + 3Ag↓
2Al + 3Cu(NO3)2 → 2Al(NO3)2 + 3Cu↓
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag↓
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu↓
Al(NO3)3 + 3NaOH → Al(OH)3↓ + 3NaNO3
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Fe(NO3)2 + 2NaOH → Fe(OH)2↓ + 2NaNO3
Cu(NO3)2 + 2NaOH → Cu(OH)2↓ + 2NaNO3
nFe = 16,8 : 56 = 0,3 (mol)
n\(Cu (NO_3)_2\) = 1. 0,1 = 0,1 (mol)
n\(AgNO_3\) = 0,5 . 0,1 = 0,05 (mol)
Thứ tự phản ứng như sau, muối của kim loại yếu hơn phản ứng trước(Cu yếu hơn Ag):
(1) Fe + Cu(NO3)2 \(\rightarrow\) Fe(NO3)2 + Cu
T 0,3 0,1
Pư 0,1 0,1 0,1 0,1
S 0,2 0 0,1 0,1
(2) Fe + 2AgNO3 \(\rightarrow\) Fe(NO3)2 + 2Ag
T 0,2 0,05
Pư 0,025 0,05 0,025 0,05
S 0,175 0 0,025 0,05
\(\rightarrow\) sau phản ứng có 0,1 mol Cu ; 0,05 mol Ag ; 0,175 mol Fe dư
m kim loại sau = 0,1.64 + 0,05.108 + 0,175.56 = 21,6 (g)
Vậy...
Ciao_