a, vì sao khối lượng 1 n.tử là do hạt nhân quyết định?
b, n.tử A có khối lượng = 2 lần KLPT oxygen . A là n.tử thuộc n.tố nào
trl giúp mình đang cần gấp
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu này dễ mà bạn
a) Do p=16
=> X là lưu huỳnh(S)
b) Ta có
p=e=16
c) dX/H=\(\frac{32}{1}=32\)
Vậy X nặng hơn nguyên tử H 32 lần
dX/O=2(lần)\
Vậy X nặng hơn O 2 lần
a, Nguyên tử của nguyên tố có 16p nên X là lưu huỳnh
Kí hiệu S
b,Vì p = e
=> e = 16
c,dX/H = 32
=> X nặng hơn nguyên tử H 32 lần
dX/O = 2
=>

lập hai hệ pt dựa vào dữ kiện đầu bài
ta có
p+n+e=116 mà p=e <=> 2p+n=49 (1)
vì số hạt mang điện nhiều hơn số hạt không mang điện là 15
=> (p+e)-n=15 mà p=e <=> 2p-n=15 (2)
từ (1) (2) => giải hệ bấm máy tính
=>p=16,n=17,e=16
Vì tổng số hạt trong ntử ntố A là 49 nên ta có: p + n + e =49
mà số p = số e => 2p + n = 49 (1)
Mặt khác: số hạt mang điện nhiều hơn số hạt không mang điện là 15 nên ta có : p+e-n=15 . mà p=e => 2p - n = 15 (2)
Từ (1) và (2) => 2p = \(\dfrac{49+15}{2}\) = 32 => p = e = 32/2 = 16
Thay p vào (1) ta được : 2.16 +n = 49=> 32+n=49 =>n=49-32=17
Vậy p=e=16; n=17

Bài 1:
- Công thức X: AB2
- Ta có: 2PA+4PB+NA+2NB=96(1)
- Mặt khác: 2PA+4PB-(NA+2NB)=32(2)
- Giải hệ ta có: PA+2PB=32(3) và NA+2NB=32(4)
- Ngoài ra: 2PA-2PB=16(5)
- Giải hệ(3,5) có PA=16(S) và PB=8(O)
-CTHH của X: SO2
Bài 2:
PA+4PB=10(1)
%A=\(\dfrac{P_A+N_A}{P_A+N_A+4\left(P_B+N_B\right)}.100=75\)(2)
-Theo đề PA=NA và PB+NB=1 nên :
(2)\(\Leftrightarrow\dfrac{P_A+P_A}{P_A+P_A+4.1}.100=75\)
\(\Leftrightarrow\dfrac{2P_A}{2P_A+4}.100=75\Leftrightarrow P_A=6\left(Cacbon:C\right)\)
-Thế (1) có PB=1(Hiđro:H)
-Công thức hợp chất: CH4

CTDC:\(Zn^{II}_x\left(SO4\right)^{II}_y\)
Theo quy tắc hóa trị ta có
\(x.II=y.II=>\frac{x}{y}=\frac{II}{II}=\frac{1}{1}\)
CTHH:ZnSO4

tổng số mol của X và Y = (42✖ 10^21)/(6✖ 10^23)=0.07mol
gọi số mol của X là a , số mol của Y là b
vì số nguyên tử Y gấp 2.5 lần số nguyên tử X nên 2.5a=b
tổng số mol của X và Y là 0.07 nên a+b=0.07(1)
thay b=2.5a vào (1) ta được 3.5a=0.07➡ a=0.02 mol➡ b=0.05 mol
vì tỉ lệ nguyên tử X và Y là 8:7 nên MX=8MY/7(2)
vì tổng số gam X và Y là 4.08 nên 0.02✖MX+0.05✖MY=4.08(3)
thay (2) vào (3) tìm được MX =56, MY =64
vậy X là Cu , Y là Fe
Fe +2HCl➡ FeCl2+H2
➡ khí B là H2
vì B có tính khử oxit nên X1 và Y1 là oxit
➡ X1 là CuO , Y1 là FeO➡ A là khí Oxi

a) Ta có : \(\left\{{}\begin{matrix}Z_B-Z_A=6\\Z_A+Z_B=28\end{matrix}\right.\)
⇔ \(\left\{{}\begin{matrix}Z_A=11\\Z_B=17\end{matrix}\right.\)
⇒ A là Natri (Na) , B là Clo (Cl)
+Cấu hình electron của A : \(1s^22s^22p^63s^1\)
số thứ tự : 11, chu kì : 3 , nhóm : IA
+Cấu hình electron của B : \(1s^22s^22p^63s^23p^5\)
số thứ tự : 17 , chu kì : 3 , nhóm : VIIA
b) -Công thức oxit cao nhất của A : \(Na_2O\)
Công thức hidroxit tương ứng : NaOH
- Công thức oxit cao nhất của B : \(Cl_2O_7\)
Công thức hidroxit tương ứng : \(HClO_4\)

Nguyên tử Y có tổng số hạt là 46 hạt : \(2Z+N=46\)
=> N= 46 - 2Z
Biết rằng trong hạt nhân nguyên tử có tổng số hạt ko quá 32 hạt.
=> Z+N \(\le\) 32
=> \(Z+46-2Z\le32\)
=> \(-Z\le-14\)
=> \(Z\ge14\) (1)
Mặt khác ta có : \(Z\le N\le1,5Z\)
=> \(Z\le46-2Z\le1,5Z\)
=> \(13,14\le Z\le15,3\) (2)
Từ (1), (2) =>\(\left[{}\begin{matrix}Z=14\\Z=15\end{matrix}\right.\Rightarrow\left[{}\begin{matrix}N=18\left(loại\right)\\N=16\left(chọn\right)\end{matrix}\right.\)
=> Z=15 , N=16
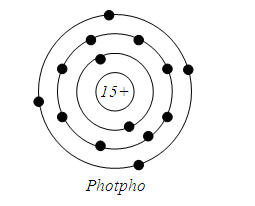
Vậy Y là Photpho (P)
Cấu hình e : 1s22s22p63s23p3
a. vì hạt nhân chiếm phần lớn khối lượng ptử, lớp vỏ electron ko đáng kể
b. => MA = 32 x 2 = 64 => A là Cu