Chia 18,24 gam hỗn hợp X gồm FeO, Fe2O3, Fe3O4 thành hai phần bằng nhau. - Phần thứ nhất tác dụng hết với dung dịch HCl (dư), thu được 17,37 gam muối khan. - Phần thứ hai tác dụng với dung dịch H2SO4 đặc nóng dư thu được V (lít) khí SO2 (ở đktc, sản phẩm khử duy nhất). Tính V?
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

28 tháng 6 2017
Đáp án : C
Coi mỗi phần hỗn hợp oxit gồm FeO và Fe2O3 với số mol là a và b
=> Muối P1 có a mol FeCl2 và 2b mol FeCl3
=> 72a + 160b = 156,8.0,5 = 78,4 và 127a + 325b = 155,4
=> a = 0,2 ; b = 0,4 mol => nCl- (muối 1) = 2,8 mol
Xét cả quá trình thì : muối phần 2 chính là muối phần 1 có 1 lượng SO42- thay thế cho Cl-
Cứ x mol SO42- thay thế cho 2x mol Cl-
=> mmuối 2 - mmuối 1 = 96x – 35,3.2x = 167,9 – 155,4 => x = 0,5 mol
=> Số mol Cl bị thay thế là 1,0 mol => số mol Cl trong muối 2 = 2,8 – 1,0 = 1,8 mol

18 tháng 4 2018
Đáp án B

Do số mol cation của 2 phần là như nhau nên tổng điện tích anion của 2 phần là như nhau Suy ra số mol Cl- trong phần 2 bằng 2,8 - 2.0,5 = 1,8 (mol)
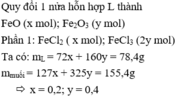

Quy đổi hỗn hợp thành Fe, O
Ta có: \(m_{P1}=m_{P2}=\dfrac{18,24}{2}=9,12\left(g\right)\)
- Phần 1:
Gọi nO = a (mol)
BTĐT: nCl = 2nO = 2a (mol)
Ta có: \(m_{muối}=m_{oxit}-m_O+m_{Cl}\)
\(\Rightarrow9,12-16a+2a.35,5=17,37\)
=> a = 0,15 (mol)
Theo BTNT: \(m_{Fe}=9,12-0,15.16=6,72\left(g\right)\)
=> \(n_{Fe}=\dfrac{6,72}{56}=0,12\left(mol\right)\)
- Phần 2:
Vì 2 phần bằng nhau nên: \(\left\{{}\begin{matrix}n_{Fe}=0,12\left(mol\right)\\n_O=0,15\left(mol\right)\end{matrix}\right.\)
Quá trình oxi hoá - khử
\(Fe^0-3e\rightarrow Fe^{+3}\\ O^0+2e\rightarrow O^{-2}\\ S^{+6}+2e\rightarrow S^{+4}\)
BTe: \(3n_{Fe}=2n_O+2n_{SO_2}\)
=> \(n_{SO_2}=\dfrac{0,12.3-0,15.2}{2}=0,03\left(mol\right)\)
=> V = 0,03.22,4 = 0,672 (l)
Quy đổi hỗn hợp thành Fe, O
Ta có: \(m_{P1}=m_{P2}=\dfrac{18,24}{2}=9,12\left(g\right)\)
- Phần 1:
Gọi \(n_O=a\left(mol\right)\)
Bảo toàn điện tích: \(n_{Cl}=2n_O=2a\left(mol\right)\)
Ta có: \(m_{muối}=m_{oxit}-m_O+m_{Cl}\)
\(\Rightarrow9,12-16a+2a.35,5=17,37\)
=> a = 0,15 (mol)
Theo BTNT: \(m_{Fe}=9,12-0,15.16=6,72\left(g\right)\)
=> \(n_{Fe}=\dfrac{6,72}{56}=0,12\left(mol\right)\)
- Phần 2:
Vì 2 phần bằng nhau nên: \(\left\{{}\begin{matrix}n_{Fe}=0,12\left(mol\right)\\n_O=0,15\left(mol\right)\end{matrix}\right.\)
Quá trình oxi hoá - khử:
\(Fe^0-3e\rightarrow Fe^{+3}\\ O^0+2e\rightarrow O^{-2}\\ S^{+6}+2e\rightarrow S^{+4}\)
BTe: \(3n_{Fe}=2n_O+2n_{SO_2}\)
=> \(n_{SO_2}=\dfrac{3.0,12+0,15.2}{2}=0,33\left(mol\right)\)
=> V = 0,33.22,4 = 7,392 (l)