Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
Phần 1 :
Gọi $n_{CuO} = a ; n_{Fe_2O_3} = b$
Ta có :
$80a + 160b = 80 : 2 = 40(1)$
$CuO + 2HCl \to CuCl_2 + H_2O$
$Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2O$
Suy ra:
$135a + 162,5.2b = 78,5(2)$
Từ (1)(2) suy ra a = 0,1 ; b = 0,2
$\%m_{CuO} = \dfrac{0,1.80}{40}.100\% = 20\%$
$\%m_{Fe_2O_3} = 80\%$
b)
Dung dịch muối gồm :
$Fe^{3+} : 2b = 0,4(mol)$
$Cu^{2+} : a = 0,1(mol)$
$Cl^- : x(mol)$
$SO_4^{2-} : y(mol)$
Bảo toàn điện tích : 0,4.3 + 0,1.2 = x + 2y
$m_{muối} = 0,4.56 + 0,1.64 + 35,5x + 96y = 84,75$
Suy ra x = 0,9 ; y = 0,25
$C_{M_{HCl}} = \dfrac{0,9}{0,5} = 1,8M$
$C_{M_{H_2SO_4}} = \dfrac{0,25}{0,5} = 0,5M$

Phương trình hoá học :
C n H 2 n + 1 COOH + NaOH → C n H 2 n + 1 COONa + H 2 O
Gọi số mol của hai axit trong hỗn hợp là x.
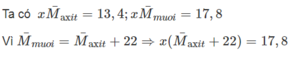
13,4 + 22x = 17,8 => x = 0,2 => số mol của mỗi axit trong hỗn hợp là 0,1
Ta có công thức của 2 axit là C a H 2 a + 1 COOH (0,1 mol)
C b H 2 b + 1 COOH (0,1 mol)
Vậy : (14a + 46)0,1 + (14b + 46)0,1 = 13,4
=> 14a + 14b = 42 => a + b = 3
a = 1; b = 2 → CH 3 COOH và C 2 H 5 COOH
m CH 3 COOH = 0,1 x 60 = 6g
m C 2 H 5 COOH = 0,1 x 74 = 7,4g
% m CH 3 COOH = 6/13,4 x 100% ≈ 44,8%
% m C 2 H 5 COOH = 100% - 44,8% = 55,2%
n NaOH = n CH 3 COOH + n C 2 H 5 COOH = 0,2 mol
V = n : C M = 0,2 : 1 = 200ml

