Cho 8,4 gam R tác dụng với O2 tạo thành 12 gam oxit
Xác định R?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi hóa trị của R là x
PTHH: \(2R+xH_2SO_4\rightarrow R_2\left(SO_4\right)_x+xH_2\uparrow\)
\(n_{H_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
Theo PTHH: \(n_R=\dfrac{2\cdot0,15}{x}=\dfrac{0,3}{x}\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{8,4}{\dfrac{0,3}{x}}=28x\left(g/mol\right)\)
Khi \(x=1\Rightarrow M_R=28\left(loai\right)\)
Khi \(x=2\Rightarrow M_R=56\left(Fe\right)\)
Khi \(x=3\Rightarrow M_R=84\left(loai\right)\)
Vậy kim loại R là Fe (II)

a, \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: R + 2HCl → RCl2 + H2
Mol: 0,15 0,3 0,15
\(M_R=\dfrac{8,4}{0,15}=56\left(g/mol\right)\)
⇒ R là sắt (Fe)
b, \(m_{ddHCl}=\dfrac{0,3.36,5.100}{15}=73\left(g\right)\)

\(2R+2nHCl\rightarrow2RCl_n+nH_2\)
.0,12/n...............0,12/n......0,06......
\(R_2O_n+2nHCl\rightarrow2RCl_n+nH_2O\)
.0,3/n......................................0,3....
\(n_{H_2O}=2n_{O_2}=0,3\left(mol\right)\)
Có : \(m=13,44=m_R+m_{R_2O_n}=\dfrac{0,12R}{n}+\dfrac{\left(2R+16n\right)0,3}{n}\)
\(\Rightarrow R=12n\)
=> R là Mg
\(n_{Al\left(I\right)}=\dfrac{3}{2}n_{H_2}=0,045\left(mol\right)\)
\(n_{Al\left(II\right)}=2n_{Al_2O_3}=\dfrac{2}{3}n_{H_2O}=\dfrac{2}{3}.2n_{O_2}=\dfrac{4}{3}n_{O_2}=\dfrac{1}{15}\left(mol\right)\)
\(\Rightarrow m_{Al}=m=3,015\left(g\right)\)

Gọi số mol Mg, R trong mỗi phần là a, b (mol)
=> 24a + b.MR = 16 (1)
* Nếu R tan trong HCl
- Phần 1:
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
a-------------------->a
2R + 2nHCl --> 2RCln + nH2
b--------------------->0,5bn
=> a + 0,5bn = 0,4 (2)
-Phần 2: \(n_{SO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: Mg + 2H2SO4 --> MgSO4 + SO2 + 2H2O
a-------------------------->a
2R + 2mH2SO4 --> R2(SO4)m + mSO2 + 2mH2O
b----------------------------->0,5bm
=> a + 0,5bm = 0,5 (3)
(3) - (2) => 0,5bm - 0,5bn = 0,1 (mol)
=> bm - bn = 0,2 => m > n
- Xét n = 1; m = 2 => b = 0,2 (mol) => a = 0,3 (mol)
(1) => MR = 44 (g/mol) => Loại
- Xét n = 1; m = 3 => b = 0,1 (mol) => a = 0,35 (mol)
(1) => MR = 76 (g/mol) => Loại
- Xét n = 2; m = 3 => b = 0,2 (mol) => a = 0,2 (mol)
(1) => MR = 56 (g/mol) => R là Fe
* Nếu R không tan trong HCl
- Phần 1:
PTHH: Mg + 2HCl --> MgCl2 + H2
0,4<--------------------0,4
=> a = 0,4 (mol)
- Phần 2:
PTHH: Mg + 2H2SO4 --> MgSO4 + SO2 + 2H2O
0,4-------------------------->0,4
2R + 2kH2SO4 --> R2(SO4)k + kSO2 + 2kH2O
\(\dfrac{0,2}{k}\)<--------------------------0,1
Có: \(m_{R\left(phần.2\right)}=16-0,4.24=6,4\left(g\right)\)
=> \(M_R=\dfrac{6,4}{\dfrac{0,2}{k}}=32k\left(g/mol\right)\)
Xét k = 2 thỏa mãn => MR = 64 (g/mol) => R là Cu

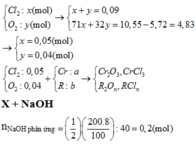
C r C l 3 + 4 N a O H → N a C r O 2 + 3 N a C l + 2 H 2 O 0 , 02 0 , 08 0 , 02 2 N a C r O 2 + 3 B r 2 + 8 N a O H → 2 N a 2 C r O 4 + 6 N a B r + 4 H 2 O 0 , 02 0 , 08 0 , 02



cho 6g một Kim loại R có hóa trị không đổi khi tác dụng với oxi tạo ra 10g oxit. Kim loại R là ?
Giải thích các bước giải:
6.0 gam R + O2 → 10 gam oxit
mO2 = 10 - 6 = 4 gam → nO2 = 0,125 mol
Theo bảo toàn e: n x nR = 0.125 X 4 → n x 6R6R = 0.5 → nRnR = 0.560.56 = 1212
Biện luận n = 2,R = 24 → Mg
⇒Kim loại R là:Mg
Gọi n là hóa trị của kim loại R cần tìm.
$4R + nO_2 \xrightarrow{t^o} 2R_2O_n$
Theo PTHH :
$n_R = 2n_{R_2O_n}$
$\Rightarrow \dfrac{8,4}{R} = 2.\dfrac{12}{2R + 16n}$
$\Rightarrow R = \dfrac{56}{3}n$
Với n = 3 thì R = 56(Fe)$
Vậy R là Fe(Sắt)