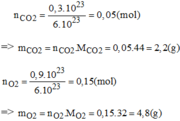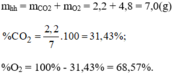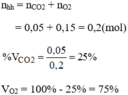Đốt cháy 2,4(g)cacbon (c)bằng 10(g) khí oxi (O2) thì thu được 8,8(g) khí cacbonic (CO2) biết khí oxi còn dư. Tính khối lượng oxi dư
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Thành phần theo khối lượng:
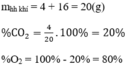
Thành phần phần trăm theo thể tích:


Khối lượng của các khí:
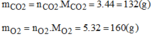
Thành phần phần trăm theo khối lượng:
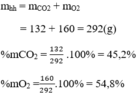
Thành phần phần trăm theo thể tích:
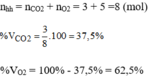

nC=4,8/12=0,4(mol)
nO2=6,72/22,4=0,3(mol)
PTHH: C+ O2 -to-> CO2
Ta có: 0,4/1 > 0,3/1
=> C dư, O2 hết, tính theo nO2
=> nCO2=nC(p.ứ)=nO2=0,3(mol)
=>nC(dư)=0,4-0,3=0,1(mol)
=>mC(dư)=0,1.12=1,2(g)
V(CO2,đktc)=V(O2,đktc)=6,72(l) (Số mol tỉ lệ thuận thể tích)

Câu 1 :
$n_C = \dfrac{4,8}{12} = 0,4(mol) ; n_{O_2} = \dfrac{7,437}{24,79} = 0,3(mol)$$
$C + O_2 \xrightarrow{t^o} CO_2$
Ta thấy :
$n_C : 1 > n_{O_2} : 1$ nên C dư
$n_{C\ pư} = n_{O_2} = 0,3(mol) \Rightarrow m_{C\ dư} = (0,4 - 0,3).12 = 1,2(gam)$
$\Rightarorw V_{CO_2} = V_{O_2} = 7,437(lít)$
Câu 2 :
$n_{Mg} = \dfrac{2,4}{24} = 0,1(mol)$
$n_{Cl_2} = \dfrac{9,916}{24,79} = 0,4(mol)$
$Mg + Cl_2 \xrightarrow{t^o} MgCl_2$
Ta thấy :
$n_{Mg} : 1 < n_{Cl_2} : 1$ nên $Cl_2$ dư
$n_{Cl_2\ pư} = n_{Mg} = 0,1(mol) \Rightarrow m_{Cl_2\ dư} = (0,4 - 0,1).71 = 21,3(gam)$
$n_{MgCl_2}= n_{Mg} = 0,1(mol) \Rightarrow m_{MgCl_2} = 0,1.95 = 9,5(gam)$

Bài 3:
\(a,m_C+m_{O_2}=m_{CO_2}\\ b,m=22-16=6\left(g\right)\)
Bài 4:
\(a,m_S+m_{O_2}=m_{SO_2}\\ b,m_{O_2}=6,4-3,2=3,2\left(g\right)\)

\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\
pthh:CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
0,2 0,4 0,4
\(V_{O_2}=0,4.22,4=8,96\left(l\right)\\
m_{H_2O}=0,4.18=7,2\left(g\right)\)

a, nO2 = 5,6/22,4 = 0,25 (mol)
PTHH: C + O2 -> (t°) CO3
Mol: 0,25 <--- 0,25 ---> 0,25
b, mCO2 = 0,25 . 44 = 11 (g)
c, LTL: 0,2 < 0,25 => O2 dư