Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Thành phần theo khối lượng:
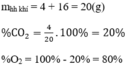
Thành phần phần trăm theo thể tích:


Khối lượng của các khí:
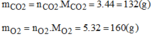
Thành phần phần trăm theo khối lượng:
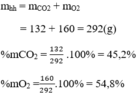
Thành phần phần trăm theo thể tích:
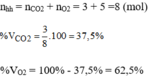

1, a, + 8.2=16 => CH4
+ 8,5 . 2 = 17 => NH3
+ 16 . 2 =32 => O2
+ 22 . 2 = 44 => CO2
b, + 0,138 . 29 \(\approx4\) => He
+ 1,172 . 29 \(\approx34\) => H2S
+ 2,448 . 29 \(\approx71\Rightarrow Cl_2\)
+ 0,965 . 29 \(\approx28\) => N

Câu 9:
1) nSO2 = 2,24 : 22,4 = 0,1 mol
nO2 = 3,36 : 22,4 = 0,15 mol
mhh = 0,1 . 64 + 0,15 . 32 = 11,2
2. nCO2 = 4,4 : 44 = 0,1 mol
nO2 = 3,2 : 32 = 0,1 mol
Vhh = (0,1 + 0,1 ) . 22,4 = 4,48 l
3. n = \(\frac{3.10^{23}}{6.10^{23}}=0,5mol\)
Câu 10 :
1. C2H5OH + 3O2 -> 2CO2 + 3H2O
2. Tỉ lệ : 1 : 3 : 2 : 3
3.

Phương trình hóa học :
2C2H6 + 7O2 -> 6H2O + 4CO2
Tỉ lệ :
2 : 7 : 6 : 4

PTHH:
\(CuO+H_2\) \(\underrightarrow{t^o}\) \(Cu+H_2O\) \(\left(1\right)\)
\(Fe_2O_3+3H_2\) \(\underrightarrow{t^o}\) \(2Fe+3H_2O\) \(\left(2\right)\)
Số mol H2 là 0,6 mol
Gọi số mol H2 tham gia pư 1 là x mol \(\left(0,6>x>0\right)\)
Số mol H2 tham gia pư 2 là \(\left(0,6-x\right)mol\)
Theo PTHH 1:
\(n_{CuO}=n_{H_2}=x\left(mol\right)\)
Theo PTHH 2:
\(n_{Fe_2O_3}=\frac{1}{3}n_{H_2}=\left(0,6-x\right):3\left(mol\right)\)
Theo bài khối lượng hh là 40g
Ta có pt: \(80x+\left(0,6-x\right)160:3=40\)
Giải pt ta được \(x=0,3\)
Vậy \(n_{CuO}=0,3\left(mol\right);n_{Fe_2O_3}=0,1\left(mol\right)\)
\(\%m_{CuO}=\left(0,3.80.100\right):40=60\%\)
\(\%m_{Fe_2O_3}=\left(0,1.160.100\right):40=40\%\)
1)
PTHH: \(2Cu+O_2\) \(\underrightarrow{t^o}\) \(2CuO\)
x x
Gọi số mol Cu phản ứng là x mol ( x >0)
Chất rắn X gồm CuO và Cu
Ta có PT: 80x + 25,6 – 64x = 28,8
Giải PT ta được x = 0,2
Vậy khối lượng các chất trong X là:
\(m_{Cu}\) = 12,8 gam
\(m_{CuO}\) = 16 gam
2)
Gọi kim loại hoá trị II là A.
PTHH: \(A+2HCl\rightarrow ACl_2+H_2\)
Số mol \(H_2\)= 0,1 mol
Theo PTHH: \(n_A=n_{H_2}\)= 0,1 (mol)
Theo bài \(m_A\) = 2,4 gam \(\Rightarrow\) \(M_A\) = 2,4 : 0,1 = 24 gam
Vậy kim loại hoá trị II là Mg

nO2= 0,2 mol.
m O2= 6,4 gam
=> tổng m H2O + CO2= 1,6 + 6,4= 8 gam .
gọi a là nCO2 => 2a là nH2O. ta có :
44a + 36a= 8 => a= 0,1 mol
=> mCO2= 4,4 gam
=>mH2O= 3,6 gam
b. nCO2= 0,1 mol => nC= 0,1 mol
nH2O= 0.2 mol => nH= 0,4 mol
nC:nH= 1:4 =>CTPT có dạng (CH4)n.
vì M_Y= 16 <=> 16n=>n=1. => CTPT của Y là CH4.

Bảo toàn khối lượng \(n_{O_2}=\frac{30,2-17,4}{32}=0,4mol\)
\(\Rightarrow V=0,4.22,4=8,96l\)

a.
C + O2 -> CO2
a......a........a
S + O2 -> SO2
b.......b.........b
=> 12a + 32b = 5,6
(a + b )32 = 9,6
giải ra: a = 0,2 ; b = 0,1
m C = 0,2 . 12 = 2,4g
m S = 0,1 .32 = 3,2 g
b.
% n SO2 = 100% - 66,67% = 33,33%
Thành phần % theo khối lượng:
Thành phần % về thể tích: