Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình: 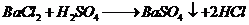
Vậy kết tủa là 

Số mol
Phương trình
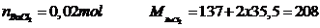

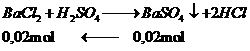
 khối lượng
khối lượng
Vậy m là 

a) Sơ đồ : CO + Fe2O3 ---> CO2 + Fe
PTHH : 6CO + 2Fe2O3 -> 6CO2 + 4Fe
b) Áp dụng định luật bảo toàn khối lượng ta có :
\(m_{CO}+m_{Fe_2O_3}=m_{CO_2}+m_{Fe}\)
c) Từ PTKL trên ta có :
8,4 + 16 = 13,2 + mFe
=> mFe = ( 8,4 + 16 ) - 13,2 = 11,2 ( g )

nMg = \(\dfrac{6}{24}=0,25\left(mol\right)\)
Pt: Mg + 2HCl --> MgCl2 + H2
...0,25........0,5......................0,25
VH2 thu được = 0,25 . 22,4 = 5,6 (lít)
mHCl đã dùng = 0,5 . 36,5 = 18,25 (g)
c) nFe2O3 = \(\dfrac{16}{160}=0,1\left(mol\right)\)
Pt: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
...................0,25 mol--> \(\dfrac{0,5}{3}\) mol
Xét tỉ lệ mol giữa Fe2O3 và H2:
\(\dfrac{0,1}{1}>\dfrac{0,25}{3}\)
Vậy Fe2O3 dư
mFe thu được sau pứ = \(\dfrac{0,5}{3}.56=9,33\left(g\right)\)

Bài I
1. Lập công thức hoá học của :
a) Nhôm(III) VÀ oxi: Al2O3
b) Natri và nhóm SO4: Na2SO4
c) Bari và nhóm OH: Ba(OH)2
2. Tính phân tử khối của NaOH và FeCl3
+) PTKNaOH = 23 + 16 + 1 = 40đvC
+) PTKFeCl3 = 56 + 3 x 35,5 = 162,5 đvC
Bài II:
1. Tính số mol của 11,2 gam sắt.
=> nFe = \(\frac{11,2}{56}=0,2\left(mol\right)\)
2. Tính số mol của 1,12 lít khí hiđro(đktc)
=> nH2 = \(\frac{1,12}{22,4}=0,05\left(mol\right)\)
3. Tìm khối lượng của 4,8 lít CO2 (đktc)
=> nCO2 = \(\frac{4,8}{22,4}=\frac{3}{14}\left(mol\right)\)
=> mCO2 = \(\frac{3}{14}.44=9,43\left(gam\right)\)
4. Tìm số mol của 11,1 gam CaCl2
=> ncaCl2 = \(\frac{11,1}{111}=0,1\left(mol\right)\)
Bài III
1. PTHH: Fe2O3 + 3H2 =(nhiệt)=> 2Fe + 3H2O
2. Ta có: nFe = \(\frac{16}{160}=0,1\left(mol\right)\)
a) Theo phương trình, nH2 = 0,1 x 3 = 0,3 (mol)
=> VH2(đktc) = \(0,3\times22,4=6,72\left(l\right)\)
b) Theo phương trình, nFe = 0,1 x 2 = 0,2 (mol)
=> mFe = 0,2 x 56 = 11,2 (gam)

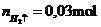
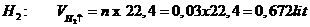

đề câu b có sai ko bn?
Theo bạn thì như nào đúng