Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) 2CO + O2 2CO2
Phản ứng này là phản ứng oxi hóa - khử (và cũng là phản ứng hóa hợp). Khí CO khi đốt là cháy được. Vai trò của co là chất khử. Phản ứng này tỏa nhiều nhiệt nên dược dùng trong luyện gang, thép.
b) CO + CuO CO2 + Cu
Phản ứng này là phản ứng oxi hóa - khử. Phản ứng này xảy ra ở nhiệt độ cao.
Vai trò của CO là chất khử. Phản ứng này dùng để điều chế Cu.
a) 2CO + O2 2CO2
Phản ứng này là phản ứng oxi hóa - khử (và cũng là phản ứng hóa hợp). Khí CO khi đốt là cháy được. Vai trò của co là chất khử. Phản ứng này tỏa nhiều nhiệt nên dược dùng trong luyện gang, thép.
b) CO + CuO CO2 + Cu
Phản ứng này là phản ứng oxi hóa - khử. Phản ứng này xảy ra ở nhiệt độ cao.
Vai trò của CO là chất khử. Phản ứng này dùng để điều chế Cu.

Phương trình hóa học:
a) S + O2 → SO2
b) C + O2 → CO2
c) 2Cu + O2 → 2CuO
d) 2Zn + O2 → 2ZnO
Oxit tạo thành là oxit axit:
SO2 axit tương ứng là H2SO3.
CO2 axit tương ứng là H2CO3.
Oxit tạo thành là oxit bazơ :
CuO bazơ tương ứng là Cu(OH)2.
ZnO bazơ tương ứng là Zn(OH)2.
Ta có các PTHH theo đề:
\(S+O_2\rightarrow^{t^0}SO_2\) SO2 là một oxit axit, có axit tương ứng là H2SO3.
\(C+O_2\rightarrow^{t^0}CO_2\) CO2 là một oxit axit, có axit tương ứng là H2CO3.
\(2Cu+O_2\rightarrow^{t^0}2CuO\) CuO là một oxit bazo, có bazo tương ứng là Cu(OH)2.
\(2Zn+O_2\rightarrow^{t^0}2ZnO\) ZnO là một oxit lưỡng tính.

Phương trình hóa học:
a) H2 (k) + Cl2 (k) → 2HCl(k) (HCl ở trạng thái khí, không màu)
b) S + H2 (k) → H2S (k) (H2S ở trạng thái khí, không màu, có mùi trứng thối)
c) H2 + Br2 → 2HBr(to) (HBr ở trạng thái khí, không màu)

Thủy tinh (có thành phần chính là Na2SiO3, CaSiO3) được sản xuất theo ba công đoạn chính:
- Trộn hỗn hợp cát, đá vôi, sôđa theo một tỉ lệ thích hợp.
- Nung hỗn hợp trong lò nung ở khoảng 900°c thành thủy tinh ở dạng nhão.
- Làm nguội từ từ thủy tinh dẻo, ép thổi thủy tinh dẻo thành các đồ vật. Các phản ứng xảy ra:
CaCO3 CaO + CO2
SiO2 + CaO CaSiO3
SiO2 + Na2CO3 Na2SiO3 + CO2
Bài 4. Sản xuất thuỷ tinh như thế nào ? Viết các phương trình hoá học của phản ứng xảy ra trong quá trình nấu thuỷ tinh.
Lời giải:
Thủy tinh (có thành phần chính là Na2SiO3, CaSiO3) được sản xuất theo ba công đoạn chính:
- Trộn hỗn hợp cát, đá vôi, sôđa theo một tỉ lệ thích hợp.
- Nung hỗn hợp trong lò nung ở khoảng 900°c thành thủy tinh ở dạng nhão.
- Làm nguội từ từ thủy tinh dẻo, ép thổi thủy tinh dẻo thành các đồ vật. Các phản ứng xảy ra:
CaCO3 CaO + CO2
SiO2 + CaO CaSiO3
SiO2 + Na2CO3 Na2SiO3 + CO2

nFe = 0,1 mol; nS = 0,05 mol
a) Phương trình phản ứng:
Fe + S → FeS (1)
nFe dư = 0,1 – 0,05 = 0,05 nên hỗn hợp chất rắn A có Fe và FeS.
Fe + 2HCl → FeCl2 + H2↑ (2)
FeS + 2HCl → FeCl2 + H2S↑ (3)
b) Dựa vào phương trình phản ứng (2) và (3), ta có:
nHCl= 0,1 + 0,1 = 0,2 mol
VHCl = 0,2 /1 = 0,2 lít.

a) Đặt công thức oxít M2On
Ptpư: M2On + nH2SO4 → M2(SO4)n + nH2O
mol 1 n 1
mddH2SO4 = n.98.100/10 = 980n gam
mdd muối = 2M + 996n (gam)
→ C% muối = (2M + 96n) : (2M + 996n) = 0,11243
→ M = 9n → M = 27 (Al)
→ Công thức oxít: Al2O3
b) ptpứ: Al2O3 ---> 2Al + 3/2O2
Al2O3 + 2NaOH ---> 2NaAlO2 + H2O
Al2(SO4)3 + 3Na2CO3 + 3H2O ---> 2Al(OH)3 + 3Na2SO4 + 3CO2

a) Đặt công thức oxít M2On
Ptpư: M2On + nH2SO4 --->M2(SO4)n + nH2O
mol 1 n 1
mddH2SO4 = n.98.100/10 = 980n gam
mdd muối = 2M + 996n (gam)
→ C% muối = (2M + 96n) : (2M + 996n) = 0,11243
→ M = 9n → M = 27 (Al)
→ Công thức oxít: Al2O3
b) ptpứ: Al2O3 ------> 2Al + 3/2O2
Al2O3 + 2NaOH --->2NaAlO2 + H2O
Al2(SO4)3 + 3Na2CO3 + 3H2O --->2Al(OH)3+ 3Na2SO4 + 3CO2

2CuO+C-->2Cu+CO2
2PbO+C-->2Pb+CO2
CO2+C-->2CO
2FeO+C-->2Fe +CO2
ỨNG DỤNG
thu đc đơn chất ra khỏi oxit
a) 2CuO+C--->2Cu+CO2
b) 2PbO+C---->2Pb+CO2
c) CO2+C--->2CO
d) FeO+C--->CO+Fe
Vai trò bạn lên mạng tìm hiểu nhé
Cacbon monoxit – Wikipedia tiếng Việt
Các phương trình hóa học:
a) С + 2CuO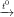 2Cu + CO2
2Cu + CO2
b) С + 2PbO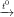 2Pb + CO2
2Pb + CO2
c) С + CO2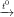 2CO
2CO
d) С + 2FeO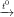 2Fe + CO2
2Fe + CO2
Các phản ứng trên dều thuộc loại phản ứng oxi hóa - khử. Vai trò của с là chất khử. Các phản ứng:
a), b) dùng điều chế kim loại.
c), d) xảy ra trong quá trình luyện gang, dùng luyện gang.