Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt :
nCaCO3 = x mol
CaCO3 -to-> CaO + CO2
x___________x
m giảm = mCaCO3 - mCaO = 33
<=> 100x - 56x = 33
<=> x = 0.75
CaCO3 -to-> CaO + CO2
0.75________0.75
mA = 100 - 0.75*100 + 0.75*56 = 67 g
H% = 75/100*100% = 75%

a)mCaCO3=500.80%=400(g) -> nCaCO3=400/100=4(mol)
PTHH: CaCO3 -to-> CaO + H2O
nCaO(LT)=nCaCO3=4(mol)
=> nCaO(TT)=4. 70%=2,8(mol)
=>mX=mCaO+ m(trơ)+ mCaCO3(chưa p.ứ)=2,8.56+100+ 1,2.100=376,8(g)
b) %mCaO= (156,8/376,8).100=41,614%

Ta có: mKCl thực tế = 61.25 . 80 :100 =49g
------> n KCl = 49 : 74,5 = 0,65 mol
a) 2KClO3 -----> 2KCl + 3O2
2 2 3
0,65 <-------- )0,65
mKClO3 = 0,65 . 122,5 = 79,625 mol

Gọi n KMnO4 = a
n KClO3 = b ( mol )
--> 158a + 122,5 b = 43,3
PTHH :
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\uparrow\)
0,9b 1,35b
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,9a 0,45a
\(\%Mn=\dfrac{55a}{43,3-32\left(0,45a+1,35b\right)}=24,103\%\)
\(\rightarrow a=0,15\)
\(b=0,16\)
\(m_{KMnO_4}=0,15.158=23,7\left(g\right)\)
\(m_{KClO_3}=0,16.122,5=19,6\left(g\right)\)

Pthh:
2KClO3--t'->2KCl+3O2
Độ giảm khối lượng chất rắn =mO2=21,65-19,2=2,45g
nO2=2,45: 32~0,0766mol
=>nKClO3 tham gia =0,0766.2:3~0,05mol.
%mKClO3 phan ung=((0,05.122,5):21,65).100%gần bằng 28,9%
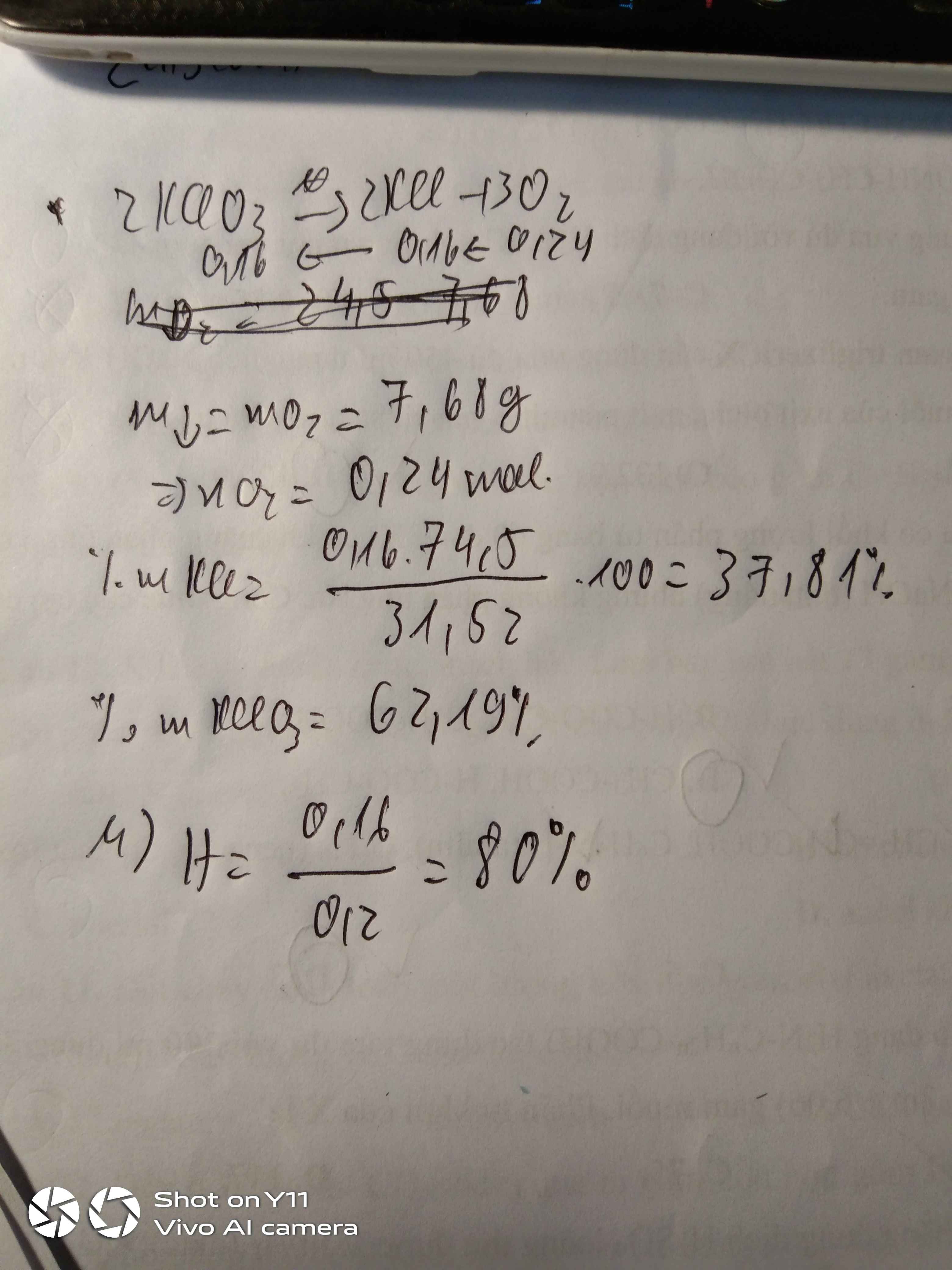
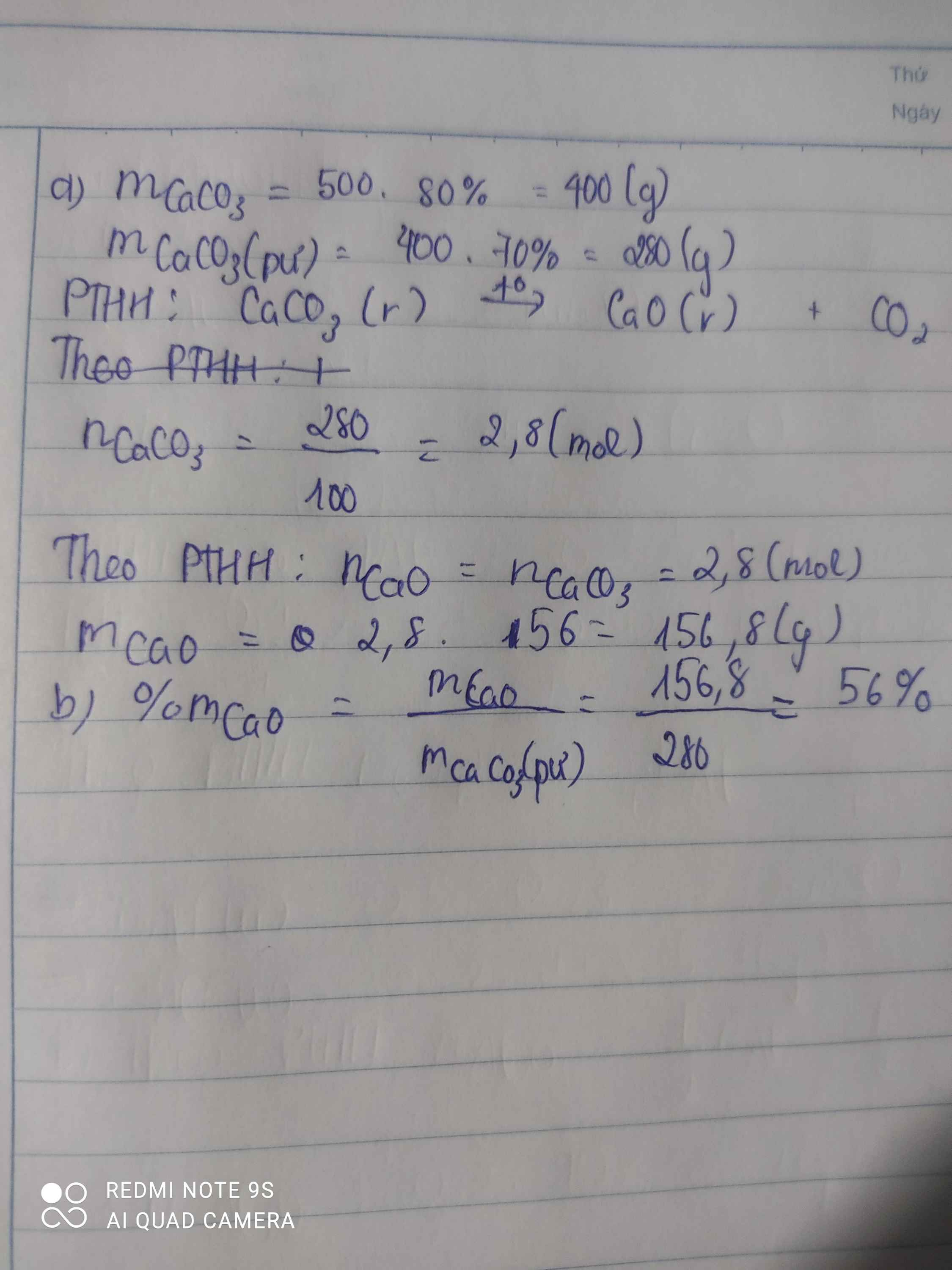
Giả sử ban đầu có 100g CaCO3
Gọi số mol CaCO3 phản ứng là a
PTHH: CaCO3 --to--> CaO + CO2
a------------->a------>a
=> mgiảm = mCO2 = 44a (g)
=> \(\dfrac{44a}{100}.100\%=20\%\)
=> a = \(\dfrac{5}{11}\left(mol\right)\)
=> \(H\%=\dfrac{\dfrac{5}{11}.100}{100}.100\%=45,45\%\)
100% - 20% = 80%