Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Pthh:
2KClO3--t'->2KCl+3O2
Độ giảm khối lượng chất rắn =mO2=21,65-19,2=2,45g
nO2=2,45: 32~0,0766mol
=>nKClO3 tham gia =0,0766.2:3~0,05mol.
%mKClO3 phan ung=((0,05.122,5):21,65).100%gần bằng 28,9%

a, PTHH: 2KClO3 --to--> 2KCl + 3O2
b, \(n_{O_2}=\dfrac{53,76}{22,4}=2,4\left(mol\right)\\ n_{O_2}=2,4.32=76,8\left(g\right)\)
Bảo toàn khối lượng: \(m_{KClO_3}=76,8+168,2=245\left(g\right)\)
c, Theo pthh: \(n_{KClO_3\left(pư\right)}=\dfrac{2}{3}n_{O_2}=\dfrac{2}{3}.2,4=1,6\left(mol\right)\\ \Rightarrow\%m_{KClO_3\left(phân.huỷ\right)}=\dfrac{1,6.122,5}{245}=80\%\)

Bài 1; Tính số mol và khối lượng KMnO4 cần thiết để điều chế được;
PTHH: 2 KMnO4 -to-> K2MnO4 + MnO2 + O2
a, 24g khí oxi
Ta có: nO2= 24/32= 0,75(mol)
=> nKMnO4= 2.nO2=2.0,75=1,5(mol)
-> mKMnO4=1,5.158=237(g)
b, 5,6 lít oxi ở đktc
nO2= 5,6/22,4=0,25(mol)
=> nKMnO4=2.nO2=2.0,25=0,5(mol)
=> mKMnO4=0,5.158=79(g)

2KClO3 => (to) 2KCl + 3O2
nO2 = 53.76/22.4 = 2.4 (mol)
=> nKCl = nKClO3 = 1.6 (mol)
mKClO3 = n.M = 122.5 x 1.6 = 196 (g)
mKCl = n.M = 74.5 x 1.6 = 119.2 (g)
mKClO3 dư = mchất rắn - mKCl = 168.2 - 119.2 = 49 (g)
mKClO3 ban đầu = mKClO3 pứ + mKClO3 dư = 49 + 196 = 245 (g)
% KClO3 đem nhiệt phân = 196x100/245 = 80%

Gọi n KMnO4 = a
n KClO3 = b ( mol )
--> 158a + 122,5 b = 43,3
PTHH :
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\uparrow\)
0,9b 1,35b
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,9a 0,45a
\(\%Mn=\dfrac{55a}{43,3-32\left(0,45a+1,35b\right)}=24,103\%\)
\(\rightarrow a=0,15\)
\(b=0,16\)
\(m_{KMnO_4}=0,15.158=23,7\left(g\right)\)
\(m_{KClO_3}=0,16.122,5=19,6\left(g\right)\)

2KClO3 -to-> 2KCl + 3O2 (1)
NaCl --đpnc--> Na +Cl2 (2)
mNaCl=25/100 .a=0,25a(g)
=>nNaCl=0,25a/58,5=0,0042a(mol)
mKClO3=a - 2,5a=0,75a(g)
=> nKClO3=0,75a/122,5=0,0061a(mol)
mchất rắn thu được=90,4/100 .a=0,904a(g)
theo (1): nKCl=nKClO3=0,0061a(mol)
=>mKCl=0,0061a.74,5=0,455a(g)
theo (2) : nNa=nNaCl=0,0042a(mol)
=>mNa=0,0042.23=0,096a(mol)
=>%mKCl =0,455a/0,904a .100=50,33(%)
%mNa=0,0966a/0,904a .100=10,68(%)

Khối lượng của các chất trong hỗn hợp ban đầu là:
\(\left\{{}\begin{matrix}m_{KClO_3}=75\%a=0,75a\\m_{NaCl}=25\%a=0,25a\end{matrix}\right.\)
\(2KClO_3\left(x\right)\rightarrow2KCl\left(x\right)+3O_2\)
Gọi số mol KClO3 bị phân hủy là x
\(\Rightarrow m_{KCl}=74,5x\left(g\right)\)
\(\Rightarrow m_{KClO_3\left(pứ\right)}=122,5x\left(g\right)\)
\(\Rightarrow m_{KClO_3\left(dư\right)}=0,75a-122,5x\left(g\right)\)
Thành phần chất rắn sau phản ứng là:
\(\left\{{}\begin{matrix}m_{NaCl}=0,25a\\m_{KCl}=74,5x\\m_{KClO_3\left(dư\right)}=0,75a-122,5x\end{matrix}\right.\)
\(\Rightarrow m_{hhspu}=0,25a+74,5x+0,75a-122,5x=a-48x\)
Theo đề bài ta có:
\(\dfrac{a-48x}{a}.100\%=90,4\%\)
\(\Leftrightarrow a=500x\)
Từ đây ta có phần trăm theo khối lượng của hh sau phản ứng là:
\(\left\{{}\begin{matrix}\%NaCl=\dfrac{0,25a}{a-48x}.100\%=\dfrac{0,25.500x}{500x-48x}.100\%=27,65\%\\\%KCl=\dfrac{74,5x}{a-48x}.100\%=\dfrac{74,5x}{500x-48x}.100\%=16,48\%\\\%KClO_3\left(dư\right)=100\%-27,65\%-16,48\%=55,87\%\end{matrix}\right.\)
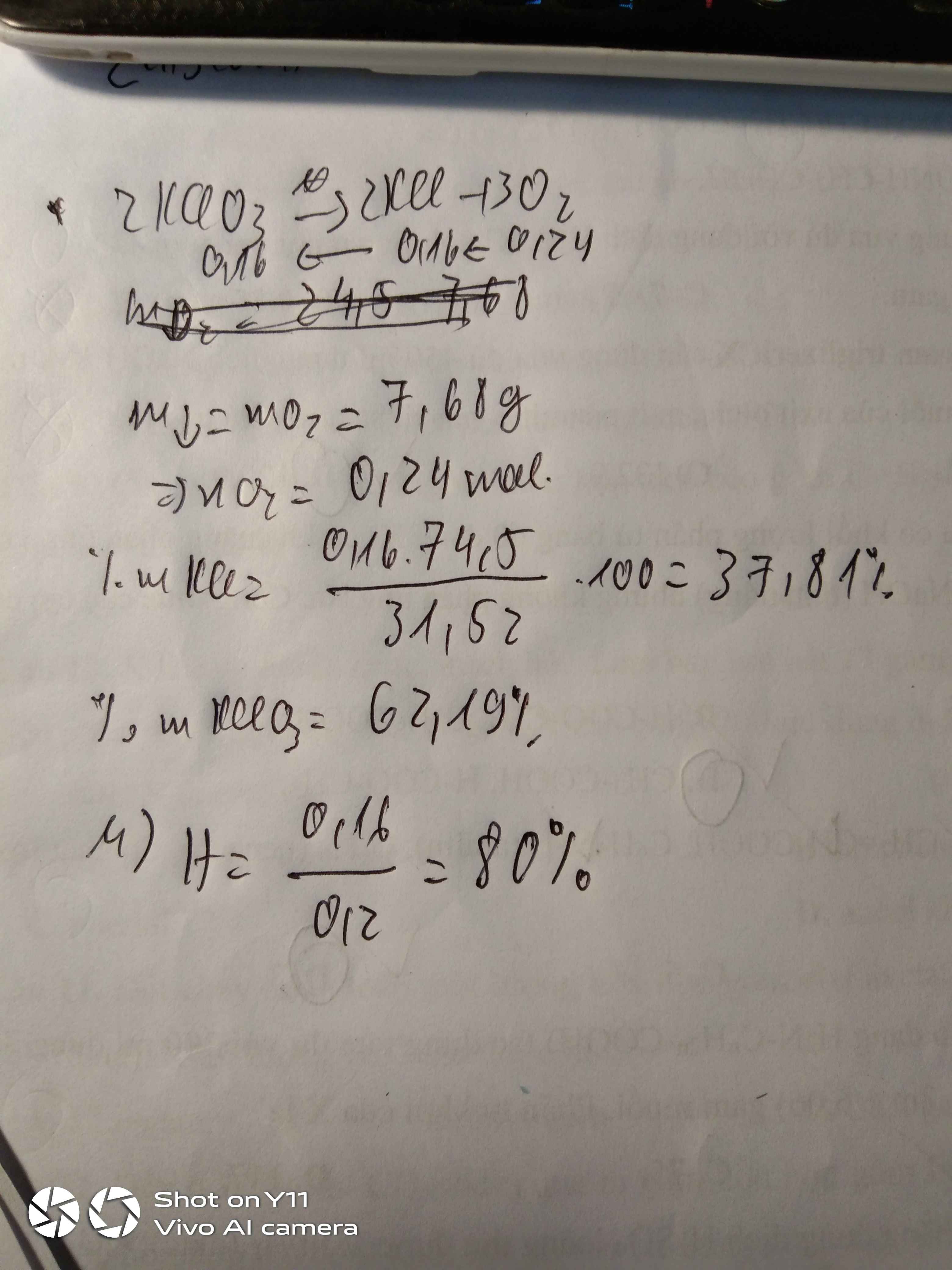

Ta có: mKCl thực tế = 61.25 . 80 :100 =49g
------> n KCl = 49 : 74,5 = 0,65 mol
a) 2KClO3 -----> 2KCl + 3O2
2 2 3
0,65 <-------- )0,65
mKClO3 = 0,65 . 122,5 = 79,625 mol
a) 2KClO3→2 KCl + 3O2