Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Gọi công thức TB của hai muối cacbonat là: M ¯ C O 3
M ¯ C O 3 → t 0 M O + C O 2 ( 1 )
Chất rắn Y ( M ¯ C O 3 ; M ¯ O )
n C O 2 ( 1 ) = 3 , 36 22 , 4 = 0 , 15 m o l
Y tác dụng với dung dịch HCl dư
M ¯ C O 3 + 2 H C l → t 0 M ¯ C l 2 + C O 2 + H 2 O ( 2 ) M ¯ O + H C l → t 0 M ¯ C l 2 + H 2 O ( 3 ) C O 2 + B a ( O H ) 2 → B a C O 3 + H 2 O ( 4 ) 2 C O 2 + B a ( O H ) 2 → B a ( H C O 3 ) 2 ( 5 ) B a ( H C O 3 ) 2 → t 0 B a C O 3 + C O 2 + H 2 O ( 6 ) n B a C O 3 ( 4 ) = 9 , 85 197 = 0 , 05 m o l n B a C O 3 ( 6 ) = 9 , 85 197 = 0 , 05 m o l
Theo PT (4,5,6): n C O 2 ( 3 ) = 0 , 15 m o l
Theo PT (1,2):
n M ¯ C O 3 = n C O 2 ( 2 ) + n C O 2 ( 1 ) = 0 , 15 + 0 , 15 = 0 , 3 m o l
Muối khan là: M ¯ C l 2
M ¯ C O 3 → M ¯ C l 2 M ¯ + 60 M ¯ + 71
0,3 mol muối cacbonat pư tạo 0,3 mol muối clorua tăng 3,3(g).
Khối lượng muối cacbonat ban đầu là: 38.15-3,3= 34,85(g)
Giá trị của m = 34,85(g)

Chọn đáp án B
Hỗn hợp X ta có thể quy đổi về CHO, COOH và C
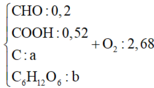
![]()
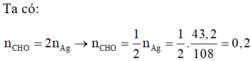
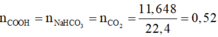
Gọi số mol C và C6H12O6 lần lượt là a, b mol.
Sau khi thêm m’ gam C6H12O6 vào m gam X rồi đốt cháy ta có:
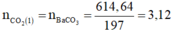
![]()
Áp dụng định luật bảo toàn H vào (1), ta có:
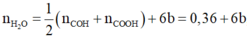
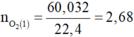
![]()
![]()


Đáp án C
Có nCHO =0,5 nAg = 0,2 mol, nCOOH = nCO2 = 0,52 mol
Vì Ba(OH)2 dư nên nCO2 = nBaCO3 =3,12 mol
Khi đốt cháy m gam X có nH2Ở đó X sinh ra = 0,5 . (nCHO + nCOOH ) = 0,5 . ( 0,2 +0,52) =0,36 mol
Có nX = 0,5.(nCHO + nCOOH ) =0,36 mol → nC =0,72
Hỗn hợp Z gồm
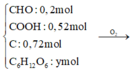
3,12 mol CO2 + ( 6y + 0,36) H2O
Bảo toàn nguyên tố O → nO2 = 3 , 12 × 2 + 6 y + 0 , 36 - 0 , 2 - 0 , 52 × 2 - 6 y 2 = 2,68 → V = 60,032 lít
Bảo toàn nguyên tố C → 0,72 + 6y = 3,12 - 0,2 - 0,52 = 2,4 → y = 0,28
m + m' =0,2. 29 +0,52. 45 + 12. 0,72 + 180 .0,28 = 88,24 gam

Đáp án C
Đặt nCO PT1 = x mol; n C O 2 P T 2 = y mol
C + H2O → t 0 CO + H2
x x mol
C + 2H2O → t 0 CO2 + 2H2
y 2y mol
→nhỗn hợp X = nCO + n C O 2 + n H 2 = 2x+ 3y= 17,92/22,4 = 0,8 mol (*)
CO2+ Ba(OH)2 → BaCO3+ H2O
n C O 2 = n B a C O 3 = 35,46/197 = 0,18 mol
→ y = 0,18 mol
Thay vào (*) ta có x = 0,13 mol
Khí thoát ra là CO (0,13 mol); H2 (x+2y = 0,49 mol)
CO + CuO → t 0 Cu + CO2 (4)
x x
H2 + CuO → t 0 Cu + H2O (5)
(x+2y) (x+2y) mol
Khối lượng chất rắn giảm chính là khối lượng oxi trong oxit tách ra
Theo PT (4,5) ta có: nO (Oxit tách ra) = nCO+ n H 2 = x+x+2y = 0,62 mol
→m = 0,62.16 = 9,92 gam

Đáp án B
Gọi công thức trung bình của hai muối ACO3 và BCO3 là MCO3
MCO3 → MO + CO2
n C O 2 = 3,36 /22,4 = 0,15 mol → n M C O 3 = 0,15 mol
Hỗn hợp Y gồm MCO3 dư và MO
MCO3 + 2HCl → MCl2 + CO2 + H2O
MO + 2HCl → MCl2 + H2O
CO2 + Ca(OH)2 dư → CaCO3 ↓ + H2O
n C a C O 3 = 15/100 = 0,15 mol
→ n M C O 3 dư = 0,15 mol
n M C O 3 ban đầu = 0,15 + 0,15 = 0,3 mol
Bảo toàn kim loại M có:
n M C O 3 = n M C l 2 = 0,3 (mol)
Bảo toàn khối lượng có:
m M C O 3 = m M C l 2 - 0,3.(71- 60) = 29,2 (gam)

Lời giải
X gồm: C4H6O2; C6H10O4; C2H4O2 và C3H8O3
Vì n C 4 H 6 O 4 = n C 2 H 4 O 2 nên ta coi 2 chất có công thức chung là C3H5O2.
Lại có C6H10O4 cũng có CT đơn giản nhất là C3H5O2.
=>Quy đổi hỗn hợp X về hỗn hợp gồm C3H5O2 và C3H8O3 với số mol lần lượt là x,y(mol)
=>73x + 92y = 13,36(g) (1)
Mặt khác ta có: n B a C O 3 = 0 , 25 ( m o l ) . Vì khi đun nóng Z lại thu được kết tủa
=>trong Z có Ba(HCO3)2
Bảo toàn nguyên tố Ba ⇒ n B a ( H C O 3 ) 2 = n B a ( O H ) 2 - n B a C O 3 = 0 , 13 ( m o l )
Bảo toàn nguyên tố C ⇒ = n C O 2 = n B a C O 3 + 2 n B a ( H C O 3 ) 2 = 0 , 51 ( m o l )
=>3x + 3y = 0,51(mol) (2).
(1) và (2) => x = 0,12(mol); y = 0,05(mol)
=>n-COOH = 0,12 (mol) => nKOH phản ứng = n H 2 O = 0,12 (mol)
Ta có chất rắn khan sau phản ứng gồm muối kali và KOH dư. Bảo toàn khối lượng ta có:
mchất rắn = m a x i t + m K O H - m H 2 O = m X - m g l i x e r o l + m K O H - m H 2 O = 14 , 44 ( g )
Đáp án A.
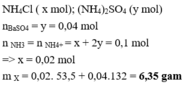
Đáp án D