
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(m_{NaCl}=\dfrac{150.10}{100}=15\left(g\right)\\ m_{H_2O}=150-15=135\left(g\right)\)
Đong 15 gam NaCl khan, 135 gam nước cho sẵn vào cốc nước. Sau đó hóa tan 15 gam NaCl vào nước, dùng đũa thủy tinh khuấy đều thu được dd như theo yêu cầu của đề bài


a)
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
n Al = 2,7/27 = 0,1 mol
n HCl =200.7,3%/36,5 = 0,4(mol)
Ta thấy:
n Al / 2 = 0,05 < n HCl / 6 = 0,067 => HCl dư
n H2 = 3/2 n Al = 0,15(mol)
=> V H2 = 0,15.22,4 = 3,36 lít
b) n HCl pư = 3n Al = 0,3(mol)
=> n HCl dư = 0,4 - 0,3 = 0,1(mol)
m dd sau pư = m Al + m dd HCl - m H2 = 2,7 + 200 - 0,15.2 = 202,4 gam
Vậy :
C% AlCl3 = 0,1.133,5/202,4 .100% = 6,6%
C% HCl dư = 0,1.36,5/202,4 .100% = 1,8%
PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
a) Ta có: \(\left\{{}\begin{matrix}n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\\n_{HCl}=\dfrac{200\cdot7,3\%}{36,5}=0,4\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{2}< \dfrac{0,4}{6}\) \(\Rightarrow\) HCl còn dư
\(\Rightarrow n_{H_2}=\dfrac{3}{2}n_{Al}=0,15\left(mol\right)\) \(\Rightarrow V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\)
b) Ta có: \(\left\{{}\begin{matrix}n_{HCl\left(dư\right)}=0,1\left(mol\right)=n_{AlCl_3}\\n_{H_2}=0,15\left(mol\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd}=m_{Al}+m_{ddHCl}-m_{H_2}=2,7+200-0,15\cdot2=202,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{HCl\left(dư\right)}=\dfrac{0,1\cdot36,5}{202,4}\cdot100\%\approx1,8\%\\C\%_{AlCl_3}=\dfrac{0,1\cdot133,5}{202,4}\cdot100\%\approx6,6\%\end{matrix}\right.\)

Tính chất hóa học :
- Tác dụng với kim loại tạo oxit bazo hoặc oxit lưỡng tính
$4Na + O_2 \xrightarrow{t^o} 2Na_2O$
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
- Tác dụng với phi kim tạo oxit trung tính, oxit axit,..
$S + O_2 \xrightarrow{t^o} SO_2$
$2C + O_2 \xrightarrow{t^o} 2CO$
- Tác dụng với một số hợp chất khác :
$2CO + O_2 \xrightarrow{t^o} 2CO_2$
$CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
$4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2$

$a\big)$
$ZnO+H_2\xrightarrow{t^o}Zn+H_2O$
$CuO+H_2\xrightarrow{t^o}Cu+H_2O$
$b\big)$
$n_{H_2}=\frac{3,92}{22,4}=0,175(2)$
Theo PT: $n_{H_2O}=n_{H_2}=0,175(mol)$
$\to y=m_{H_2O}=0,175.18=3,15(g)$
BTKL:
$m_M+m_{H_2}=m_N+m_{H_2O}$
$\to m_N=14,1+0,175.2-3,15=11,3(g)$
$\to x=11,3(g)$
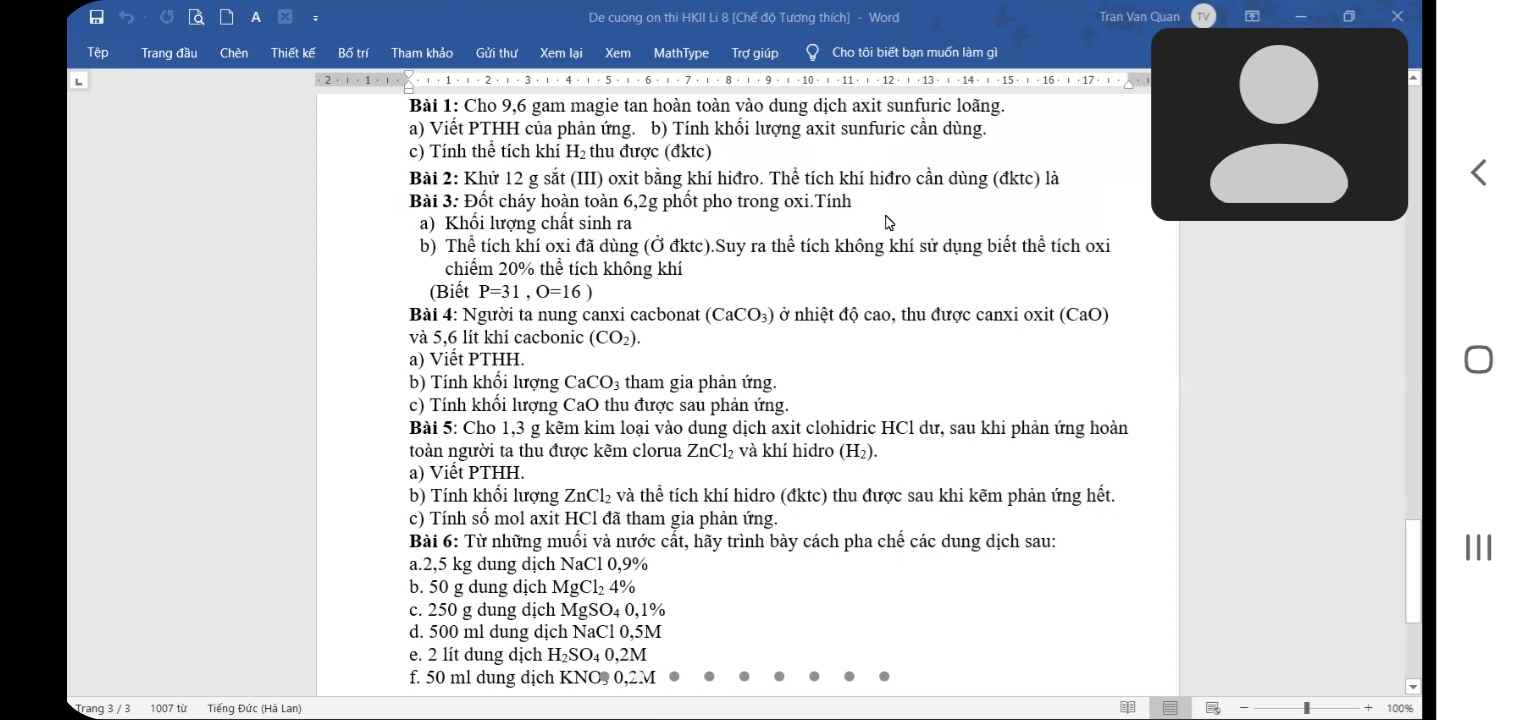






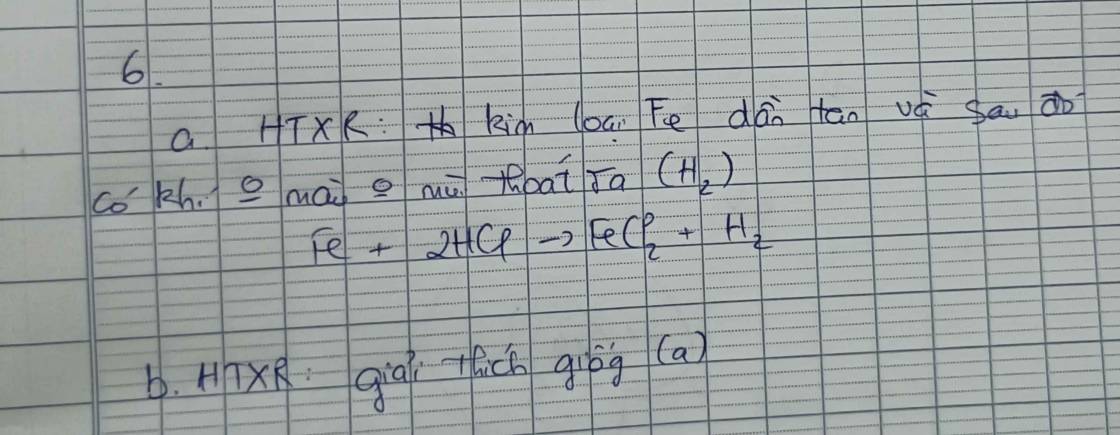


 mọi người giúp mình câu 35 với ạ . Mai em thi rùi huhu
mọi người giúp mình câu 35 với ạ . Mai em thi rùi huhu

Ta có: \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
PT: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
__0,2___0,25___0,1 (mol)
a, mP2O5 = 0,1.142 = 14,2 (g)
b, VO2 = 0,25.22,4 = 5,6 (l)
⇒Vkk = 5,6 : 20% = 28 (l)
Bạn tham khảo nhé!
a) n P = 6,2/31 = 0,2(mol)
$4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
n P2O5 = 1/2 n P = 0,1 mol
m P2O5 = 0,1.142 = 14,2(gam)
b) n O2 = 5/4 n P = 0,25(mol)
=> V O2 = 0,25.22,4 = 5,6 lít
=> V không khí = V O2 / 20% = 5,6/20% = 28 lít