Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C.
Phản ứng tự oxi hóa khử là phản ứng trong đó 1 nguyên tố trong 1 chất vừa thể hiện tính oxi hóa vừa thể hiện tính khử.
(1) 2H2O2 → 2H2O + O2 (nguyên tố O).
(3) Cl2 + KOH → KCl + KClO + H2O (nguyên tố Cl).
(5) NO2 + H2O → HNO3 + NO (nguyên tố N).

Đáp án C
3 C u + 8 H N O 3 → 3 C u N O 3 2 + 2 N O + 4 H 2 O

Đáp án A
Định hướng tư duy giải
3 C n H 2 n + 2 K M n O 4 + 2 H 2 O → 3 C n H 2 n O H 2 + 2 K O H + 2 M n O 2

Đáp án B
Do Cl vừa tăng số OXH khi thành Cl+5, v a giảm khi thành Cl-

Đáp án B
► Ta có quá trình cho - nhận e:
8 × || Al → Al3+ + 3e
3 × || 2N+5 + 8e → 2N+4 (N2O)
⇒ điền hệ số vào phương trình, chú ý không điền vào HNO3
(vì N+5 ngoài vai trò oxi hóa còn giữ lại làm môi trường NO3):
● 8Al + HNO3 → 8Al(NO3)3 + 3N2O + H2O.
Bảo toàn nguyên tố Nitơ ⇒ hệ số của HNO3 là 30.
Bảo toàn nguyên tố Hidro ⇒ hệ số của H2O là 15.
||⇒ 8Al + 30HNO3 → 8Al(NO3)3 + 3N2O + 15H2O

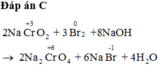
Đáp án B
Xác định số oxi hóa:
Cl20 + KOH→ t0 KCl-1 + KCl+5O3 + H2O
Quá trình cho - nhận electron:
Cl0 + e → Cl-1 (1); Cl0→ Cl+5 + 5e (2).
Thăng bằng electron:
5 x (1) + 1 x (2) => 6Cl0 → 5Cl-1 + Cl+5.
Điền hệ số vào phương trình:
3Cl2 + KOH → t0 5KCI + KClO3 + H2O
Bảo toàn nguyên tố K 6KOH.
Bảo toàn nguyên tố H => 3H2O.
Do đó:
3Cl2+6KOH → t0 5KCI + KCIO3 + 3H2O