Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi \(\left\{{}\begin{matrix}n_{C_nH_{2n+2}}=a\left(mol\right)\\n_{C_mH_{2m}}=b\left(mol\right)\end{matrix}\right.\)
=> \(a+b=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(n_{CO_2}=\dfrac{33,6}{22,4}=1,5\left(mol\right)\)
\(n_{H_2O}=\dfrac{30,6}{18}=1,7\left(mol\right)\)
Bảo toàn C: an + bm = 1,5
=> 2an + 2bm = 3 (1)
Bảo toàn H: 2an + 2a + 2bm = 3,4 (2)
(2) - (1) => 2a = 0,4
=> a = 0,2 (mol)
\(\%V_{C_nH_{2n+2}}=\dfrac{0,2}{0,5}.100\%=40\%\)
\(\%V_{C_mH_{2m}}=100\%-40\%=60\%\)

Phương trình hóa học :
CH 3 COO C n H 2 n + 2 + (3n+4)/2 O 2 → (n+2)C O 2 + (n+2) H 2 O
C n H 2 n + 2 OH + 3n/2 O 2 → nC O 2 + (n+1) H 2 O
Áp dụng định luật bảo toàn khối lượng :
=> 22,2 + m O 2 = 44 + 19,8 => m O 2 = 41,6g
Sau phản ứng: m O = 44/44 x 32 + 19,8/18 x 16 = 49,6g
Vậy khối lượng oxi có trong este và ancol là : 49,6 - 41,6 = 8 (gam).
Theo phương trình hoá học khi đốt cháy este thu được n CO 2 = n H 2 O còn khi đốt cháy ancol số mol H 2 O lớn hơn số mol C O 2 .
=> n ancol = n H 2 O - n CO 2 = 1,1 - 1 = 0,1 mol
Vậy khối lượng oxi trong este là : 8 - 16.0,1 = 6,4g
=> n este = 6,4/32 = 0,2 mol
=> 0,2(n+2) + 0,1n = 1
=> 2n + 4 + n = 10 => n = 2

Khi cho hỗn hợp A qua dung dịch brom dư, có phản ứng :
C 2 H 2 + 2 Br 2 → C 2 H 2 Br 4
Vì phản ứng xảy ra hoàn toàn và có hai khí thoát ra khỏi dung dịch brom, nên hai khí đó là CH 4 và C n H 2 n + 2
Theo đề bài V C 2 H 2 tham gia phản ứng là : 0,896 - 0,448 = 0,448 (lít).
Vậy số mol C 2 H 2 là 0,448/22,4 = 0,02 mol
Gọi số mol của CH 4 là X. Theo bài => số mol của C n H 2 n + 2 cũng là x.
Vậy ta có : x + x = 0,448/22,4 = 0,02 => x = 0,01
Phương trình hoá học của phản ứng đốt cháy hỗn hợp :
2 C 2 H 2 + 5 O 2 → 4 CO 2 + 2 H 2 O
CH 4 + 2 O 2 → CO 2 + 2 H 2 O
2 C n H 2 n + 2 + (3n+1) O 2 → 2n CO 2 + 2(n+1) H 2 O
Vậy ta có : n CO 2 = 0,04 + 0,01 + 0,01n = 3,08/44 => n = 2
Công thức phân tử của hiđrocacbon X là C 2 H 6

Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(2CH_3COOH+CaCO_3\rightarrow\left(CH_3COO\right)_2Ca+CO_2+H_2O\)
\(2C_nH_{2n+1}COOH+CaCO_3\rightarrow\left(C_nH_{2n+1}COO\right)_2Ca+CO_2+H_2O\)
Theo PT: \(n_X=2n_{CO_2}=0,4\left(mol\right)\)
Gọi CTPT chung của X là: \(C_{\overline{n}}H_{2\overline{n}+1}COOH\)
\(\Rightarrow M_{C_{\overline{n}}H_{2\overline{n}+1}COOH}=\dfrac{21,2}{0,4}=53\left(g/mol\right)\)
\(\Rightarrow12\overline{n}+2\overline{n}+1+45=53\Rightarrow\overline{n}=0,5\)
Mà: 1 trong 2 axit là CH3COOH
→ Axit còn lại là HCOOH.
Vậy: CTPT cần tìm là HCOOH.

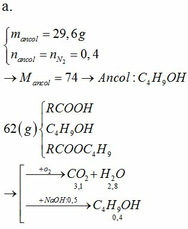
n CO2 = 0,6 mol => m CO2 = 0,6 . 44 = 26,4 g
n H2O = 0,8 mol
=> n ancol = 0,8 – 0,6 = 0,2 mol
Bảo toàn khối lượng : m Oxy + m hỗn hợp = m CO2 + m H2O
=> m oxy + 15,2 = 26,4 + 14,4 => m Oxy = 25,6 g => n O2 = 0,8 mol
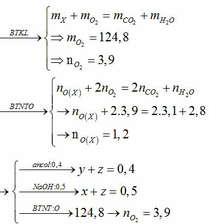
Bảo toàn nguyên tố oxy : n O ( trong hỗn hợp ) + 2 n O2 ( đốt cháy ) = n CO2 . 2 + n H2O
=> 2 n axit + n ancol + 0,8 . 2 = 0,8 + 0,6 .2
=> n Axit = 0,1 mol ( vì n ancol = 0,2 mol )
=> n axit . ( n + 1 ) + n ancol . m = n CO2
=> 0,1 . (n + 1 ) + 0,2 . m = 0,6
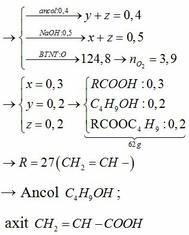
=> n +2 m = 5
TH1 m = 2 thì n = 1 TH2: m = 1 thì n = 3
C2H5OH và CH3COOH ( loại vì có số C giống nhau đều là 2 C )
hoặc C3H7COOH và CH3OH ( chọn )
C3H7COOH + CH3OH → C3H7COOCH3 + H2O
0,1 0,2 => 0,1 mol
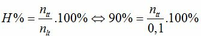
=> n thực tế = 0,09 mol
=> m C3H7COOCH3 = 0,09 . 102 = 9,18 g
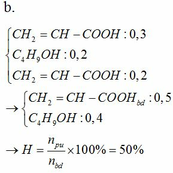
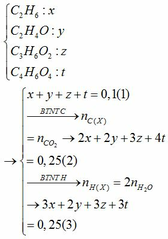
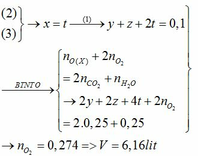
C2H6 + \(\frac{7}{2}\)O2 \(\underrightarrow{to}\) 2CO2 + 3H2O (1)
CnH2n + \(\frac{3n}{2}\)O2 \(\underrightarrow{to}\) nCO2 + nH2O (2)
\(n_{CO_2}=\frac{13,44}{22,4}=0,6\left(mol\right)\)
\(n_{H_2O}=\frac{12,6}{18}=0,7\left(mol\right)\)
Gọi x,y lần lượt là số mol của C2H6 và CnH2n
Theo Pt1: \(n_{CO_2}=2n_{C_2H_6}=2x\left(mol\right)\)
Theo Pt2: \(n_{CO_2}=nn_{C_nH_{2n}}=ny\left(mol\right)\)
Ta có: \(23+ny=0,6\) (*)
Theo Pt1: \(n_{H_2O}=3n_{C_2H_6}=3x\left(mol\right)\)
Theo PT2: \(n_{H_2O}=nn_{C_nH_{2n}}=ny\left(mol\right)\)
Ta có: \(3x+ny=0,7\) (**)
Từ (*)(**) ta có: \(\left\{{}\begin{matrix}2x+ny=0,6\\3x+ny=0,7\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\ny=0,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=\frac{0,4}{n}\end{matrix}\right.\)
Vậy \(n_{C_2H_6}=0,1\left(mol\right)\Rightarrow m_{C_2H_6}=0,1\times30=3\left(g\right)\)
\(n_{C_nH_{2n}}=\frac{0,4}{n}\left(mol\right)\Rightarrow m_{C_nH_{2n}}=14n\times\frac{0,4}{n}=\frac{5,6n}{n}\left(g\right)\)
Ta có: \(M_{hh}=\frac{m_{hh}}{n_{hh}}=\frac{8,6}{x+y}=\frac{8,6}{0,1+\frac{0,4}{n}}=\frac{30+14n}{2}\)
\(\Rightarrow17,2=8,6+1,4n+\frac{12}{n}\)
\(\Leftrightarrow1,4n+\frac{12}{n}-8,6=0\)
\(\Leftrightarrow1,4n^2-8,6n+12=0\)
\(\Leftrightarrow\left[{}\begin{matrix}n=4\\n=\frac{3}{1,4}\left(loại\right)\end{matrix}\right.\)
Vậy CTHH là C4H8
em làm phức tạp quá :3