Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{AgNO_3}=0,2.0,4=0,08\left(mol\right)\)
\(n_{Zn}=\dfrac{3,9}{65}=0,06\left(mol\right)\)
Gọi số mol Cu ban đầu là a (mol)
Gọi số mol Cu pư là b (mol)
PTHH: Cu + 2AgNO3 --> Cu(NO3)2 + 2Ag
b------>2b--------->b--------->2b
=> Rắn sau pư chứa \(\left\{{}\begin{matrix}Cu:a-b\left(mol\right)\\Ag:2b\left(mol\right)\end{matrix}\right.\)
=> 64(a - b) + 108.2b = 7
=> 64a + 152b = 7 (1)
dd sau pư chứa \(\left\{{}\begin{matrix}Cu\left(NO_3\right)_2:b\left(mol\right)\\AgNO_3:0,08-2b\left(mol\right)\end{matrix}\right.\)
- Nếu Zn tan hết:
\(n_{Zn\left(NO_3\right)_2}=n_{Zn}=0,06\left(mol\right)\)
Mà \(n_{NO_3^-}=0,08\left(mol\right)\)
=> Vô lí
=> Zn không tan hết
PTHH: Zn + 2AgNO3 --> Zn(NO3)2 + 2Ag
(0,04-b)<-(0,08-2b)------------>(0,08-2b)
Zn + Cu(NO3)2 --> Zn(NO3)2 + Cu
b<-------b--------------------->b
=> Rắn sau pư gồm \(\left\{{}\begin{matrix}Ag:0,08-2b\left(mol\right)\\Cu:b\left(mol\right)\\Zn:0,02\left(mol\right)\end{matrix}\right.\)
=> 108(0,08 - 2b) + 64b + 0,02.65 = 6,14
=> b = 0,025 (mol)
=> a = 0,05 (mol)
m = 0,05.64 = 3,2 (g)

\(Mg>Fe\) => `Mg` phản ứng trước
\(Mg+Cu^{2+}\rightarrow Mg^{2+}+Cu^o\)
x----->x-------------------->x
\(Fe+Cu^{2+}\rightarrow Fe^{2+}+Cu^o\)
y----->y----------------->y
Giả sử nếu \(Cu^{2+}\) chuyển hết thành \(Cu^o\)
\(\Rightarrow n_{Cu^o}=n_{Cu^{2+}}=n_{kt}\)
Có \(n_{Cu^{2+}}=0,2.1=0,2\left(mol\right)\)
\(n_{kt}=\dfrac{15,6}{64}=0,24375\left(mol\right)>0,2\left(mol\right)\)
\(\Rightarrow\)Giả sử sai, kim loại Fe trong hỗn hợp X còn dư
Theo đề có: \(m_{Fe.dư}=m_{kt}-m_{Cu}=15,6-0,2.64=2,8\left(g\right)\)
Ta có hệ phương trình:
\(\left\{{}\begin{matrix}24x+56y=9,2-2,8=6,4\\x+y=0,2\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,15\\y=0,05\end{matrix}\right.\)
a. Trong X có:
\(\left\{{}\begin{matrix}m_{Mg}=24.0,15=3,6\left(g\right)\\m_{Fe}=56.0,05+2,8=5,6\left(g\right)\end{matrix}\right.\)
b
Y: \(\left\{{}\begin{matrix}n_{MgSO_4}=x=0,15\left(mol\right)\\n_{FeSO_4}=y=0,05\left(mol\right)\end{matrix}\right.\)
\(MgSO_4+2NaOH\rightarrow Mg\left(OH\right)_2+Na_2SO_4\)
0,15--------------------->0,15
\(FeSO_4+2NaOH\rightarrow Fe\left(OH\right)_2+Na_2SO_4\)
0,05-------------------->0,05
\(m_{kt}=m_{Mg\left(OH\right)_2}+m_{Fe\left(OH\right)_2}=0,15.58+0,05.90=13,2\left(g\right)\)

nMg = 3,6/24 = 0,15 mol; nFeCl3 = 0,25.1 = 0,25 mol
Mg + 2FeCl3 → MgCl2 + 2FeCl2
0,125dư 0,025←0,25 → 0,125 → 0,25 (mol)
Mg + FeCl2 → MgCl2 + Fe
0,025→0,025 →0,025→0,025 (mol)
Vậy chất rắn sau phản ứng là Fe: nFe = 0,025 mol
=> m = mFe = 0,025.56 = 1,4 (gam)
Dung dịch X sau phản ứng gồm:
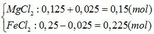
Nồng độ của các chất trong dung dịch X:
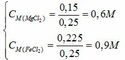

Ta có: \(n_{CuSO_4}=0,3\left(mol\right)\)
a, PT: \(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\)
______0,2____0,3_________________0,3 (mol)
b, \(m_{Al}=0,2.27=5,4\left(g\right)\)
c, \(m_{Cu}=0,3.64=19,2\left(g\right)\)
Bạn tham khảo nhé!

Ta thấy \(n_{NO3}=0,08 mol< n_{Zn}=0,09 mol=>Zn\) dư và muối trong dung dịch sau cùng là 0,04 mol Zn(NO3)2
Bảo toàn khối lượng: mZn + ,my = \(m_{dd cuối}\) +\(m_{rắn cuối}\)
=> mY = 0,04.189 + 10,53 – 5,85 = 12,24g
Bảo toàn khối lượng : mCu + mdd AgNO3 = mX + mY
=> mCu = m = 7,76 + 12,24– 0,08.170 = 6,4g.

a)nFe=0,04
nAgNO3=0,02
nCu(NO3)2=0,1
Fe + 2AgNO3 ----> Fe(NO3)2 + 2Ag
0,04.......0,02
0,01.......0,02..................................0,2
0,03.......0
Fe + CuNO3 ----> Fe(NO3)2 + Cu
0,03.....0,1
0,03.....0,03................................0,3
0
mY=mAg + mCu= 4,08
11,34g