Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Kim loại nhóm IIA, có mức oxi hóa = +2 trong hợp chất
nH2 = 0,03 mol
Gọi X là kí hiệu chung của 2 kim loại
X + 2HCl → XCl2 + H2
0,03 ← 0,03 (mol)
⇒ M = 55,6
MCa = 40 < 55,67 < MSr = 88

Đáp án B
Số mol H2 thu được là: n H 2 = 4 , 48 22 , 4 = 0 , 2 m o l
Gọi M là kim loại chung cho hai kim loại nhóm IIA
Hai kim loại nhóm IIA đều hóa trị II => M cũng hóa trị II
Sơ đồ phản ứng: M 0 + H C + 1 l → + M C l 2 + 2 + H 2 0
Các quá trình nhường, nhận electron:
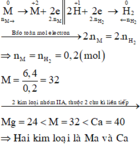

Đáp án B
Áp dụng phương pháp khối lượng mol trung bình, ta có
M = ![]() = 32
= 32
24 = M1 < 32 < M2 = 40

Đáp án B
Hướng dẫn Áp dụng phương pháp khối lượng mol trung bình, ta có
![]()
→ 24= M1 < 32 <M2 = 40

Đáp án A
Hướng dẫn Gọi công thức chung của hai kim loại là M = a mol
M + 2HCl ® MCl2 + H2
(mol): a 2a a
Số mol H2 = 0,15 mol nên a = 0,15 mol
Ta có: Ma = 4,4 ® M = 29,33
A và B là 2 kim loại nằm ở 2 chu kỳ liên tiếp thuộc nhóm IIA nên A là Mg và B là Ca

Gọi nguyên tử khối trung bình của 2 kim loại cần tìm là R
\(R+2HCl\rightarrow RCl_2+H_2\\ n_R=n_{H_2}=0,075\left(mol\right)\\ \Rightarrow M_R=\dfrac{2,2}{0,075}=29,33\\ \Rightarrow2kimloạicầntìmlà:Mg,Ca\)

\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Gọi M là hh 2 kim loại ở 2 chu kì liên tiếp
\(M+2HCl\rightarrow MCl_2+H_2\)
\(n_M=n_{H2}=0,15\left(mol\right)\)
\(M_M=\dfrac{4,4}{0,15}=29,33\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow M_{Mg}=24< 29,33< M_{Ca}=40\)
Vậy 2 kim loại cần tìm là Mg va Ca

Gọi công thức của hai kim loại cần tìm là A và B
công thức trung bình của hai kim loại là \(\overline{R}\)
PTHH : \(\overline{R}+H_2SO_4-->\overline{R}SO_4+H_2\uparrow\)
Theo PTHH : \(n_{\overline{R}}=n_{H_2}=\dfrac{22,4}{22,4}=1\left(mol\right)\)
\(\Rightarrow M_{\overline{R}}=\dfrac{36}{1}=36\) (g/mol)
Có : \(M_A< M_R=36< M_B\)
Mà : A và B thuộc hai chu kì liên tiếp
=> \(\left\{{}\begin{matrix}A:Mg\\B:Ca\end{matrix}\right.\)
Vậy ...

Đáp án A
Hướng dẫn Thay thế hỗn hợp kim loại bằng một kim loại tương đương ![]()
Số mol H2 = 0,09 (mol)
![]() + H2SO4 →
+ H2SO4 → ![]() SO4 + H2
SO4 + H2
(mol) 0,09 ![]() 0,09
0,09
![]()
=> Mg =24< 29,33 < 40=Ca
X, Y là Mg, Ca

\(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
Gọi công thức chung 2 kim loại là R
PTHH: \(R+2HCl\rightarrow RCl_2+H_2\)
0,03<------------------0,03
=> \(M_R=\dfrac{1,67}{0,03}=55,67\left(g/mol\right)\)
Mà 2 kim laoij ở 2 chu kì liên tiếp nhóm IIA
=> 2 kim loại là Ca, Sr
Gọi CT chung của 2 kim loại là R
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: R + 2HCl ---> RCl2 + H2
0,03<------------------0,03
=> \(M_R=\dfrac{1,67}{0,03}=\dfrac{167}{3}\) (g/mol)
Mà 2 kim loại này thuộc chu kì liên tiếp nhau trong nhóm IIA trong bảng tuần hoàn => 2 kim loại này là Ca và Sr