
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{KMnO_4}=\dfrac{15,8}{158}=0,1\left(mol\right)\\ 2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\\ n_{Cl_2}=\dfrac{5}{2}.0,1=0,25\left(mol\right)\\ V_{Cl_2\left(đkc\right)}=0,25.24,79=6,1975\left(l\right)\)

\(X:C_2H_5OH,A:C_2H_4,Y:-\left(CH_2-CH_2\right)-_n\\ \left(1\right)\left(C_6H_{10}O_5\right)_n+nH_2O->nC_6H_{12}O_6\\ \left(2\right)C_6H_{12}O_6-lên.men.rượu->2C_2H_5OH+2CO_2\\ \left(3\right)C_2H_5OH-H_2SO_4đ,t^0C->C_2H_4+H_2O\\ \left(4\right)nC_2H_4-t^0,p,xt->-\left(CH_2-CH_2\right)-_n\)

Gọi số mol của FeO và CuO lần lượt là x, y (x, y > 0)
Phần 1: FeO + 2HCl ➝ FeCl2 + H2O
CuO + 2HCl ➝ CuCl2 + H2O
Từ phương trình => \(\frac{127x}{2}\) + \(\frac{135y}{2}\) = 26,2 (1)
Phần 2: 2FeO + 4H2SO4 ➝ Fe2(SO4)3 + 4H2O + SO2
CuO + H2SO4 ➝ CuSO4 + H2O
Từ phương trình => 100x + 80y = 36 (2)
Từ (1), (2) suy ra: x = 0,2; y=0,2
=> m = mFe + mCuO = 27,2 g

Theo gt ta có: $n_{CO_2/(1)}=0,1(mol);n_{CO_2/(2)}=0,15(mol)$
Gọi số mol HCl và Na2CO3 lần lượt là a;b(mol)
$Na_2CO_3+2HCl\rightarrow 2NaCl+CO_2+H_2O$
$Na_2CO_3+HCl\rightarrow NaHCO_3+NaCl$
$NaHCO_3+HCl\rightarrow NaCl+H_2O+CO_2$
Dựa vào 3 phản ứng ta nhận xét là thí nghiệm nào cho lượng CO2 ít hơn chính là nhỏ từ từ HCl và Na2CO3
Do đó ta có:
+, Trường hợp 1: $\frac{a}{2}=0,1;a-b=0,15$
Giải hệ ta được $a=0,2;b=0,05$ (vô lý)
+, Trường hợp 2: $b=0,1;a-b=0,15$
Giải hệ ta được $a=0,25;b=0,1$ (Thỏa mãn)
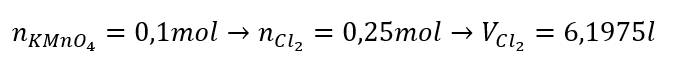
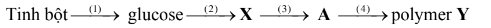
Em nhập đủ đề vào nha