Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{KL\left(mỗi.phần\right)}=\dfrac{1}{2}.15,6=7,8\left(g\right)\)
- Phần 1:
\(n_{SO_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
PTHH:
\(Zn+2H_2SO_{4\left(đ,nóng\right)}\rightarrow ZnSO_4+SO_2\uparrow+2H_2O\left(1\right)\\ Cu+2H_2SO_{4\left(đ,nóng\right)}\rightarrow CuSO_4+SO_2\uparrow+2H_2O\left(2\right)\\ 2Al+6H_2SO_{4\left(đ,nóng\right)}\rightarrow Al_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\left(3\right)\)
Theo PTHH (1,2, 3): \(n_{H_2O}=n_{H_2SO_4}=2n_{SO_2}=2.0,35=0,7\left(mol\right)\)
Áp dụng ĐLBTKL:
\(m_{KL}+m_{H_2SO_4}=m_{muối.sunfat}+m_{SO_2}+m_{H_2O}\)
=> mmuối sunfat = 7,8 + 0,7.98 - 0,35.64 - 0,7.18 = 41,4 (g)
\(\rightarrow m_{SO_4^{2-}}=41,4-7,8=33,6\left(g\right)\\ n_{SO_4^{2-}}=\dfrac{33,6}{96}=0,35\left(mol\right)\)
- Phần 2:
PTHH:
\(2Zn+O_2\underrightarrow{t^o}2ZnO\\ 2Cu+O_2\underrightarrow{t^o}2CuO\\ 4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(n_{O^{2-}}=n_{SO_4^{2-}}=0,35\left(mol\right)\\ \rightarrow m_{O^{2-}}=0,35.16=5,6\left(g\right)\\ \rightarrow m=5,6+7,8=13,4\left(g\right)\)

Bài 1:
TN1: moxit = 78,4 (g)
Gọi số mol H2SO4 pư là a (mol)
=> \(n_{H_2O}=a\left(mol\right)\) (Bảo toàn H)
Theo ĐLBTKL: \(m_{oxit}+m_{H_2SO_4}=m_{muối}+m_{H_2O}\)
=> 78,4 + 98a = 190,4 + 18a
=> a = 1,4 (mol)
=> \(n_O=n_{H_2O}=1,4\left(mol\right)\)
=> mkim loại = moxit - mO = 78,4 - 1,4.16 = 56 (g)
TN2:
Gọi \(\left\{{}\begin{matrix}n_{HCl}=x\left(mol\right)\\n_{H_2SO_4}=y\left(mol\right)\end{matrix}\right.\)
Bảo toàn H: \(n_{H_2O}=\dfrac{x+2y}{2}=1,4\left(mol\right)\)
=> x + 2y = 2,8 (1)
Có: \(m_{muối}=m_{kim.loai}+m_{Cl}+m_{SO_4}\)
=> 175,4 = 56 + 35,5x + 96y
=> 35,5x + 96y = 119,4 (2)
(1)(2) => x = 1,2; y = 0,8
Vậy số mol H2SO4 trong Y là 0,8 (mol)
Bài 2:
Gọi số mol Fe trong 15,8 gam X là a (mol)
TN1:
Bảo toàn Fe: \(n_{FeCl_2}=a\left(mol\right)\)
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
=> nHCl = 1,2 (mol)
Theo ĐLBTKL: mkim loại + mHCl = mmuối + mH2
=> mmuối = 15,8 + 1,2.36,5 - 0,6.2 = 58,4 (g)
TN2:
Bảo toàn Fe: \(n_{FeCl_3}=a\left(mol\right)\)
Khối lượng muối tăng: 61,95 - 58,4 = 3,55 (g)
=> \(m_{FeCl_3}-m_{FeCl_2}=3,55\)
=> 162,5a - 127a = 3,55
=> a = 0,1 (mol)
\(\%m_{Fe}=\dfrac{0,1.56}{15,8}.100\%=35,443\%\)

1/2m hỗn hợp= 39,2
m muối tăng= mSO4-mCl
do nso4(2-)=1/2ncl-(bảo toàn điện tích hoặc có thể viết pt ra là thấy)
83,95-77,7=96.1/2.ncl-35,5ncl
ncl bị thay thế là 0,5
có ở phần 77,7. có btkluong 39,2+36,5.2.a=77.7+18a(a là n h20)
a=0,7 ----- tổng ncl = 1,4
n kloai là 77,7-1,4.35.5=28 ----- nfeo là x fe2o3 y (ở nửa phần) có 56x+112y=28......72x+160y=39,2
x=0,1 y=0,2
%feo=18,36...... fe203=81,64%
b, ncl còn lại=nhcl=1,4-0,5=0,9
nso4=1/2ncl=0.25=nh2so4
CM=(0,25+0,9)/0,5=2,3
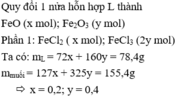

Gọi số mol của FeO và CuO lần lượt là x, y (x, y > 0)
Phần 1: FeO + 2HCl ➝ FeCl2 + H2O
CuO + 2HCl ➝ CuCl2 + H2O
Từ phương trình => \(\frac{127x}{2}\) + \(\frac{135y}{2}\) = 26,2 (1)
Phần 2: 2FeO + 4H2SO4 ➝ Fe2(SO4)3 + 4H2O + SO2
CuO + H2SO4 ➝ CuSO4 + H2O
Từ phương trình => 100x + 80y = 36 (2)
Từ (1), (2) suy ra: x = 0,2; y=0,2
=> m = mFe + mCuO = 27,2 g