Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1 :
\(CT:P_xO_y\)
Ta có :
\(\dfrac{m_P}{m_O}=\dfrac{31}{24}\Rightarrow\dfrac{31x}{16y}=\dfrac{31}{24}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(CT:P_2O_3\)

1)Khí sau phản ứng gồm :
CO : a(mol)
CO2:b(mol)
Bảo toàn nguyên tố với C: a + b = \(\dfrac{6,72}{22,4} = 0,3(mol)\)(1)
\(M_{khí} = 20.2 = 40(đvC)\)
Ta có : 28a + 44b = (a + b).40(2)
Từ (1)(2) suy ra : a = 0,075; b = 0,225
\(CO + O_{oxit} \to CO_2\\ n_{O(oxit)} = n_{CO_2} = 0,225(mol)\\ m_{Fe} + m_O = m_{oxit}\\ \Rightarrow n_{Fe} = \dfrac{13,05-0,225.16}{56}=0,16875(mol)\)
Ta thấy : \(\dfrac{n_{Fe}}{n_O} = \dfrac{0,16875}{0,225} = \dfrac{3}{4}\)
Vậy oxit cần tìm : Fe3O4
2) \(\%V_{CO_2} = \dfrac{0,225}{0,225+0,075}.100\% = 75\%\)

PTHH: AxOy + yCO --to--> xA + yCO2
Có: nCO(dư) + nCO2 = nCO(bd) = \(\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Mà \(\dfrac{28.n_{CO\left(dư\right)}+44.n_{CO_2}}{n_{CO}+n_{CO_2}}=20,4.2=40,8\)
=> nCO2 = 0,048 (mol)
\(n_{A_xO_y}=\dfrac{2,784}{x.M_A+16y}\left(mol\right)\)
AxOy + yCO --to--> xA + yCO2
=> \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{2,784y}{x.M_A+16y}=0,048\left(mol\right)\left(1\right)\\n_A=\dfrac{2,784x}{x.M_A+16y}\left(mol\right)\end{matrix}\right.\)
(1) => \(M_A=\dfrac{42y}{x}=>\dfrac{y}{x}=\dfrac{M_A}{42}\) (2)
PTHH: 2A + 2nHCl --> 2ACln + nH2
=> \(n_{H_2}=\dfrac{1,392xn}{x.M_A+16y}=0,036\left(mol\right)\)
=> \(1,392n=0,036.M_A+\dfrac{0,576y}{x}\) (3)
(2)(3) => MA = 28n
Xét n = 1 => L
Xét n = 2 => MA = 56 (Fe) => \(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
Xin cảm ơn mọi người đã đọc câu hỏi này nhưng em đã nghĩ ra đáp án cho bài tập này rồi ạ

Sơ đồ phản ứng: ZnO, CuO → C Zn, Cu
Zn + 2HCl → Zn Cl 2 + H 2
n H 2 = 2,24/22,4 = 0,1 mol
n Zn = 0,1 mol
Theo đề bài, ZnO, CuO có tỷ lệ số mol là 1:1 nên Zn và Cu cũng có tỉ lệ số mol 1:1
=> n Cu = n Zn = 0,1 mol
m CuO = 8g; m ZnO = 8,1g

Trong hỗn hợp khí, Gọi $n_{CO} = a(mol) ; n_{CO_2} = b(mol)$
Ta có :
$a + b = \dfrac{1,344}{22,4} = 0,06(mol)$
$28a + 44b = (a + b)9.4$
Suy ra a = b = 0,03
$CO + O_{oxit} \to CO_2$
$n_O = n_{CO_2} = 0,03(mol)$
$\Rightarrow n_{Fe} = \dfrac{1,6 - 0,03.16}{56} = 0,02(mol)$
$n_{Fe} : n_O = 0,02 : 0,03 = 2 : 3$
Vậy oxit là $Fe_2O_3$
Khí thu được gồm CO dư và CO2.
PT: \(Fe_xO_y+yCO\underrightarrow{t^o}xFe+yCO_2\)
Ta có: \(n_{CO\left(banđau\right)}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{CO\left(dư\right)}=a\left(mol\right)\\n_{CO_2}=b\left(mol\right)\end{matrix}\right.\)
⇒ a + b = 0,06 (1)
Mà: Tỉ khối hhk so với He bằng 9
⇒ 28a + 44b = 9.4.0,06 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,03\left(mol\right)\\b=0,03\left(mol\right)\end{matrix}\right.\)
⇒ nCO (pư) = 0,03 (mol)
Theo PT: \(n_{Fe_xO_y}=\dfrac{1}{y}n_{CO}=\dfrac{0,03}{y}\left(mol\right)\)
\(\Rightarrow M_{Fe_xO_y}=\dfrac{1,6}{\dfrac{0,03}{y}}=\dfrac{160}{3}y\left(g/mol\right)\)
\(\Rightarrow56x+16y=\dfrac{160}{3}y\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Vậy: Oxit đó là Fe2O3.
Bạn tham khảo nhé!

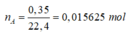
M A = m A n A = 1 0,015625 = 64 g / m o l
- Tìm số mol nguyên tử S, O trong phân tử A
Cứ 1 mol phân tử A có:
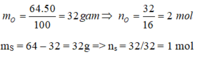
Suy ra trong 1 phân tử A có 1S và 2O, công thức của A là SO 2
Đáp án: C


19,2 < R < 35,2
R là S
Xác định được: ROx là SO2 và ROx+1 là SO3
Đặt số mol của SO2 là a, số mol của SO3 là b
Ta có: a + b = 1,25 và 64a + 80b = 84
a = 1 ; b = 0,25
%V(SO2) = 80%
%V(SO3) = 20%
X đề sai
Y :
Vì ở đktc hai khí này có khối lượng như nhau .
\(M_Y=M_{CO_2}=44\left(\dfrac{g}{mol}\right)\)
Gọi CTHH của X là \(N_xO_y\)
\(\Leftrightarrow14x+16y=44\)
Giai phương trình được x = 2;y = 1
Vậy CTHH của hợp chất là N2O .