Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi công thức hidrocacbon là CxHy
CxHy+O2\(\rightarrow\)CO2+H2O
Sau khi đốt thu được O2 dư, CO2 và H2O
Sau khi làm lạnh thu được 375ml gồm O2 dư và CO2
(H2O bị ngưng tụ)
Dẫn qua KOH thì CO2 phản ứng
CO2+2KOH\(\rightarrow\)K2CO3+H2O
\(\rightarrow\)Khí thu được là O2 dư 175ml
\(\rightarrow\)VCO2=375-175=200ml
Ta có x=VCO2/VCxHy=200/50=4
Ban đầu có 500ml O2, dư 175ml
\(\rightarrow\)O2 phản ứng 500-175=325ml
Theo bảo toàn O: 2VO2=2VCO2+VH2O
\(\rightarrow\)2.325=2.200+VH2O
\(\rightarrow\)VH2O=250ml
\(\rightarrow\)y=2VH2O/VCxHy=2.250/50=10
\(\rightarrow\)Công thức là C4H10

- Thí nghiệm 1: Cho mẫu Na vào cốc đựng cồn 10oC
- Hiện tượng: Mẫu Na tan dần, tạo thành giọt tròn chạy trên bề mặt chất lỏng và có khí không màu thoát ra.
- Giải thích: Drượu etylic10oC = \(\frac{10.0,8+90.1}{100}=0,98\left(\frac{g}{ml}\right)\) => Drượu etylic 10oC > DNa
Do vậy nên Na phản ứng vs rượu và nước ở trên bề mặt chất lỏng , phản ứng toả nhiệt làm Na nóng chảy vo tròn lại, Khí H2 tạo ra làm cho Na chạy trên bề mặt chất lỏng rồi tan dần
- Thí nghiệm 2: Cho mẫu Na vào cốc đựng rượu etylic khan
- Hiện tượng: Mẫu Na lơ lửng trong rượu , tan dần và có bọt khí k màu thoát ra
- Giải thích: Do: DC2H5OH < DNa , nên Na chìm trong rượu, phản ứng vs rượu làm Na tan dần, Khí H2 tạo ra lực đẩy làm Na lơ lửng trong rượu
- PTHH:
2Na(r) + 2H2O → 2NaOH(dd) + H2 ↑
2Na(r) + 2C2H5OH → 2C2H5ONa + H2 ↑
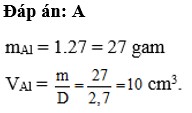


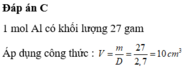
1 mol nhôm (nhiệt độ, áp suất trong phòng thí nghiệm) khối lượng riêng 2,7 g/cm3 có thể tích tương ứng là :
A. 12 cm3
B. 10 cm3
C. 13 cm3
D. 11 cm3
B nha
tính m(nhôm)=n.M=1.27=27(g)
=>V=m/D=27/2,7=10(l)=10cm3
ok nha