đặt cốc A đựng dd HCl và cốc B đựng dd H2SO4 loãng vào 2 đĩa cân sao cho cân ở ví trí cân bằng ,sau đó làm thí nghiệm như sau : -Cho 25,44 g Na2CO3 vào cốc đựng dd HCl -Cho 3,24 g kim loại M hoá trị 3 vào cốc đựng dd H2SO4 a, M là kim loại nào? b,Tính nồng độ phần trăm các muối thu được ,nếu khối lượng của mỗi dd HCl và H2SO4 khi cân thăng bằng là 160 g .Biết phản ứng xảy ra hoàn toàn
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Trước và sau phản ứng, cân vẫn ở vị trí cân bằng => lượng khí thoát ra là như nhau
Fe+ 2HCl \(\rightarrow\) FeCl2+ H2
nFe= \(\frac{a}{56}\)mol = nH2
2Al+ 3H2SO4\(\rightarrow\)Al2(SO4)3+ 3H2
nAl= \(\frac{b}{27}\)mol \(\Rightarrow\) nH2=\(\frac{b}{18}\)mol
Lượng khí thoát ra bằng nhau
\(\frac{a}{56}=\frac{b}{18}\)
\(\rightarrow\frac{a}{b}=\frac{56}{18}=\frac{28}{9}\)

Khi đổ 2 cốc vào cốc mới thì tỉ lệ dầu và nước ở 2 cốc mới là:
(2+3) : (1+1)= 5:2
Nhớ vốt cho mềnh nhé

a)
Cho Zn :
- Viên kẽm tan dần , sủi bọt khí không màu
Cho ZnO :
- Chất rắn tan dần
Cho Al2O3
- Chất rắn tan dần
\(2NaOH+Zn+2H_2O\rightarrow Na_2ZnO_2+2H_2\)
\(2NaOH+ZnO\rightarrow Na_2ZnO_2+H_2O\)
\(2NaOH+Al_2O_3\rightarrow2NaAlO_2+H_2O\)
b) Ban đầu không có hiện tượng gì. Sau một thời gian, dung dịch chuyển dần sang màu hồng. Sau đó mất màu ngay lập tức.
\(NaOH+HCl\rightarrow NaCl+H_2O\)

Đáp án A
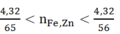
→ 0,0664 < nFe, Zn < 0,077
Ta thấy chỉ có Zn và Fe phản ứng hết với CuSO4 mà nFe, Zn < nCuSO4 nên Zn và Fe phản ứng hết.
⇒ CuSO4 dư → Kết tủa chỉ có Cu
hay