Chỉ dùng thêm quỳ tím, hãy nhận biết các dung dịch sau: H2SO4, BaCl2, KCl,NaOH
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(a,\) Trích mẫu thử, cho quỳ tím vào các mẫu thử:
- Hóa đỏ: \(H_2SO_4,HCl\)
- Hóa xanh: \(NaOH\)
- Ko đổi màu: \(BaCl_2\)
Cho \(BaCl_2\) vào nhóm quỳ hóa đỏ, sau p/ứ tạo KT trắng là \(H_2SO_4\) còn ko ht là \(HCl\)
\(H_2SO_4+BaCl_2\to BaSO_4\downarrow+2HCl\)
\(b,\) Trích mẫu thử, cho quỳ tím vào các mẫu thử:
- Hóa đỏ: \(H_2SO_4\)
- Hóa xanh: \(Ba(OH)_2,NaOH\)
- Ko đổi màu: \(NaCl\)
Cho \(H_2SO_4\) vào nhóm quỳ hóa xanh, tạo KT trắng là \(Ba(OH)_2\), còn có p/ứ xảy ra nhưng ko quan sát đc hiện tượng là \(NaOH\)
\(Ba(OH)_2+H_2SO_4\to BaSO_4\downarrow+2H_2O\)
a, quỳ tím chuyển đỏ➝ h2so4,hcl gọi đây là nhóm A
quỳ tím chuyển xanh➝NAOH
Còn lại là BACL2
Cho nhóm A tác dụng với bacl2, chất nào tác dụng tạo thành kết tủa trắng là h2so4 còn chất kia là hcl

a) Cho quỳ tím vào từng mẫu thử
Làm quỳ hóa xanh : Ba(OH)2, KOH (Nhóm 1)
Làm quỳ không đổi màu : KCl, K2SO4 (Nhóm 2)
Cho lần lượt 2 chất của nhóm 1 vào nhóm 2
+ Xuất hiện kết tủa => Chất nhóm 1 là Ba(OH)2, chất nhóm 2 là K2SO4
+ Không có hiện tượng => Chất nhóm 1 là KOH, chất nhóm 2 là KCl
b) Cho quỳ tím vào từng mẫu thử
+ Hóa xanh : Ba(OH)2, NaOH
+ Hóa đỏ : H2SO4, HCl
+ Không đổi màu : Na2SO4
Cho Na2SO4 vừa nhận vào 2 chất làm quỳ hóa xanh
+ Kết tủa : Ba(OH)2
Ba(OH)2 + Na2SO4 -----------> BaSO4 + 2NaOH
+ Không hiện tượng : NaOH
Cho dung dịch Ba(OH)2 vừa nhận vào 2 chất làm quỳ hóa đỏ
Kết tủa : H2SO4
Ba(OH)2 + H2SO4 -----------> BaSO4 + 2H2O
+ Không hiện tượng : HCl
Ba(OH)2 + 2HCl -----------> BaCl2 + 2H2O

a. Cho quỳ tím vào từng mẫu thử
+ Quỳ hóa đỏ: H2SO4
+ Quỳ hóa xanh: Ba(OH)2, NaOH
+ Quỳ không đổi màu: KCl
Cho dung dịch H2SO4 đã nhận vào 2 mẫu làm quỳ hóa xanh
+ Kết tủa:Ba(OH)2
\(H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2H_2O\)
+ Không hiện tượng: NaOH
\(H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\)
b. Cho quỳ tím vào từng mẫu thử
+ Quỳ hóa đỏ: H2SO4 , HCl
+ Quỳ hóa xanh: NaOH
+ Quỳ không đổi màu: BaCl2
Cho dung dịch BaCl2 đã nhận vào 2 dung dịch làm quỳ hóa đỏ
+ Kết tủa: H2SO4
\(H_2SO_4+BaCl_2\rightarrow BaSO_4+2HCl\)
+ Không hiện tượng: HCl

Hãy nêu phương pháp hóa học để nhận biết các kim loại sau:
Al, Fe, Cu. Gợi ý: dùng dung dịch kiềm nhận ra Al, dùng dd HCl nhận ra Fe vì Fe đúng trước H còn lại là Cu
Cho dung dịch NaOH dư vào các mẫu thử
+ Tan : Al
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
+ Không tan : Fe, Cu
Cho dung dịch HCl dư vào 2 mẫu thử còn lại
+ Tan : Fe
Fe + 2HCl → FeCl2 + H2
+ Không tan : Cu
Chỉ dùng thêm quỳ tím, hãy nhận biết các dung dịch sau:
a.1) H2SO4, NaOH, HCl, BaCl2
Cho quỳ tím vào từng dung dịch
+ Hóa đỏ : H2SO4, HCl
+ Hóa xanh : NaOH
+ Không đổi màu : BaCl2
Cho dung dịch BaCl2 vừa nhận vào 2 dung dịch làm quỳ tím hóa đỏ
+ Kết tủa : H2SO4
BaCl2 + H2SO4 ⟶ 2HCl + BaSO4
+ Không hiện tượng: HCl

Nhúng giấy quỳ tím lần lượt vào dung dịch mẫu thử. Nhận ra:
- Dung dịch NaOH, Na2SO3 : quỳ hóa xanh (nhóm 1)
- Dung dịch H2SO4 : quỳ hóa đỏ
- Dung dịch Na2SO4,BaCl2 : quỳ không đổi màu (nhóm 2)
Cho H2SO4 vào nhóm 1 nhận ra Na2SO3 vì có khí thoát ra
Na2SO3 + H2SO4 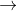 Na2SO4 + SO2 + H2O
Na2SO4 + SO2 + H2O
Chất còn lại là NaOH không hiện tượng.
- Cho Na2SO3 vào nhóm 2 nhận ra BaCl2 vì xuất hiện kết tủa trắng.
BaCl2 + Na2SO3 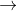 BaSO3 + 2NaCl
BaSO3 + 2NaCl
Ba dung dịch còn lại không hiện tượng
- Cho BaCl2 vào 3 dung dịch còn lại nhận ra Na2SO4 vì có kết tủa trắng xuất hiện
BaCl2 + H2SO4 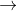 BaSO4 + 2HCl
BaSO4 + 2HCl

Dùng quỳ tím nhận biết được $NH_4HSO_4$, $H_2SO_4$ do làm quỳ hóa đỏ (Nhóm 1)
Dùng quỳ nhận biết được $Ba(OH)_2$ do làm quỳ hóa xanh
$BaCl_2;NaCl$ làm quỳ hóa tím (Nhóm 2)
Dùng $Ba(OH)_2$ nhỏ vào nhóm 1. Chất vừa tạo khí vừa tạo kết tủa là $NH_4HSO_4$. Chất chỉ tạo kết tủa là $H_2SO_4$
Dùng $H_2SO_4$ nhận biết chất ở nhóm 2. Chất tạo kết tủa là $BaCl_2$. Không cho hiện tượng là $NaCl$

Trích mẫu thử
Cho quỳ tím vào các mẫu thử
- chất nào làm quỳ tím hóa đỏ là H2SO4
- chất nào làm quỳ tím hóa xanh là NaOH
Cho dung dịch NaOH vừa nhận được vào hai mẫu thử còn lại :
- chất nào tạo kết tủa đen là AgNO3
2AgNO3 + 2NaOH → Ag2O↓ + H2O + 2NaNO3
- chất nào không có hiện tượng gì là BaCl2
- Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào quỳ tím.
+ Quỳ hóa đỏ: H2SO4
+ Quỳ hóa xanh: NaOH
+ Quỳ không đổi màu: BaCl2, KCl (1)
- Cho mẫu thử nhóm (1) pư với dd H2SO4 vừa nhận biết được.
+ Có tủa trắng: BaCl2
PT: \(H_2SO_4+BaCl_2\rightarrow2HCl+BaSO_{4\downarrow}\)
+ Không hiện tượng: KCl
- Dán nhãn.
Quỳ tím:
+ Đỏ: H2SO4
+ Xanh: NaOH
+ không hiện tượng : BaCl2 , KCl
Cho dd Axit vừa nhận biết được vào 2 dd còn lại:
+ Kết tủa : BaCl2
+ Không hiện tượng: KCl