Cho luồng khí CO dđi qua ống sứ đựng \(m\) gam Fe2O3 ở nhiệt độ cao, sau một thời gian, thu được 6,72 gam hỗn hợp X gồm X gồm 4 chất rắn khác nhau. Hòa tan hoàn toàn X vào dung dịch HNO3 dư, thu được 0,4958 lít (đkc) khí Y duy nhất có tỉ khối so với H2 bằng 15. Xác định giá trị của \(m\)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
CO + m gam Fe2O3 → 6,72 gam hỗn hợp gồm 4 chất rắn khác nhau.
m gam hỗn hợp + HNO3 dư → 0,02 mol NO
Bản chất của phản ứng là quá trình nhường nhận electron:
C+2 → C+4 + 2e
N+5 + 3e → N+2
Theo bảo toàn electron 2 × nCO = 3 × nNO → nCO = 3 × 0,02 : 2 = 0,03 mol.
CO + Fe2O3 → 6,72 gam hỗn hợp + CO2
nCO2 = nCO = 0,03 mol.
Theo bảo toàn khối lượng:
mFe2O3 = mhỗn hợp + mCO2 - mCO = 6,72 + 0,03 × 44 - 0,03 × 28 = 7,2 gam

Đáp án A
Quy đổi hỗn hợp X gồm Fe và O
mX = 56nFe + 16nO = 10,44 (1)


Đáp án B
Sơ đồ phản ứng: CO + Fe2O3
→ m1 gam Y+ HNO3 dư→ Fe(NO3)3+ NO
Ta có: nNO = 0,448/22,4 = 0,02 mol
- Quá trình cho e:
C+2 → C+4+ 2e
0,03← 0,06
- Quá trình nhận e:
NO3-+5+ 3e+ 4H+→ NO + 2H2O
0,06← 0,02 mol
Áp dụng định luật bảo toàn e:
ne cho = ne nhận = 0,06 mol → nCO = 0,03 mol
→ VCO = 0,672 lít
Ta có: nO (oxit tách ra) = nCO phản ứng = 0,03 mol
→m1 = m – mO (oxit tách ra) = m- 0,03.16 = m- 0,48 (gam)
Ta có:
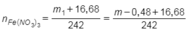
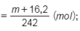
![]()
Theo bảo toàn nguyên tố Fe ta có:
n F e ( N O 3 ) 3 = 2 . n F e 2 O 3
→ m + 16 , 2 242 = 2 m 160 →m = 8 gam→m1 = m- 0,48 = 7,52 gam

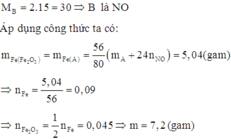
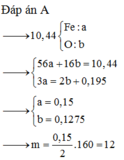


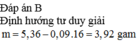
Quy đổi X thành \(\left\{{}\begin{matrix}Fe:x\left(mol\right)\\O:y\left(mol\right)\end{matrix}\right.\)
`=> 56x + 16y = 6,72(2)`
\(M_Y=15.2=30\left(g/mol\right)\Rightarrow Y:NO\\ n_{NO}=\dfrac{0,4958}{24,79}=0,02\left(mol\right)\)
`BTe: 3x - 2y = 0,02.3 = 0,06(2)`
`(1),(2)=>x=0,09;y=0,105`
`=>` \(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=0,045\left(mol\right)\)
`=> m = 0,045.160=7,2(g)`