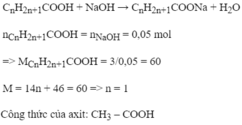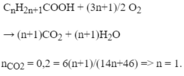Axit X có công thức CnH2n+1COOH (n >=0, nguyên; X có tính chất hóa học tương tự axit axetic). Tiến hành phản ứng este hóa giữa X và C2H5OH (có xúc tác H2SO4 đặc) thu được este Z. Sau phản ứng tách lấy hỗn hợp Y được 29,6 gam gồm este Z, axit X dư và C2H5OH dư. Chia hỗn hợp Y thành hai phần bằng nhau: Phần một phản ứng vừa đủ với 125 ml dung dịch NaOH 1M thu được dung dịch chứa m gam muối và 6,9 gam rượu. Đem đốt cháy hoàn toàn phần hai bằng khí oxi dư thu được 29,7 gam CO2 và 13,5 gam H2O. a) Viết các phương trình hóa học xảy ra và tìm công thức cấu tạo của X, Z. b) Tìm m và tính hiệu suất phản ứng este hóa.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
(III) sai vì axit no, đa chức có dạng là CnH2n + 2 - x(COOH)x
(V) sai vì axit đơn chức, no là CnH2nO2 (n ≥ 1)
Có 3 CTC đúng là (I), (II), (IV) → Chọn D.

Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PT: \(2CH_3COOH+CaCO_3\rightarrow\left(CH_3COO\right)_2Ca+CO_2+H_2O\)
\(2C_nH_{2n+1}COOH+CaCO_3\rightarrow\left(C_nH_{2n+1}COO\right)_2Ca+CO_2+H_2O\)
Theo PT: \(n_X=2n_{CO_2}=0,4\left(mol\right)\)
Gọi CTPT chung của X là: \(C_{\overline{n}}H_{2\overline{n}+1}COOH\)
\(\Rightarrow M_{C_{\overline{n}}H_{2\overline{n}+1}COOH}=\dfrac{21,2}{0,4}=53\left(g/mol\right)\)
\(\Rightarrow12\overline{n}+2\overline{n}+1+45=53\Rightarrow\overline{n}=0,5\)
Mà: 1 trong 2 axit là CH3COOH
→ Axit còn lại là HCOOH.
Vậy: CTPT cần tìm là HCOOH.

Gọi số mol của rượu, axit trong mỗi phần là a, b (mol)
- Phần 1:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: 2CnH2n+1OH + 2Na --> 2CnH2n+1ONa + H2
a---------------------------------->0,5a
2CmH2m+1COOH + 2Na --> 2CmH2m+1COONa + H2
b----------------------------------------->0,5b
=> 0,5a + 0,5b = 0,15 (1)
- Phần 2: \(n_{CO_2}=\dfrac{39,6}{44}=0,9\left(mol\right)\)
Bảo toàn C: an + b(m+1) = 0,9
=> an + bm + b = 0,9 (2)
- Phần 3:
PTHH: CnH2n+1OH + CmH2m+1COOH -H2SO4(đ),to-> CmH2m+1COOCnH2n+1 + H2O
Este có CTPT là Cm+n+1H2m+2n+2O2
=> m + n = 4 (*)
Ta có: \(n_{este\left(tt\right)}=\dfrac{5,1}{102}=0,05\left(mol\right)\)
Nếu hiệu suất là 100% => \(n_{este\left(lý.thuyết\right)}=\dfrac{0,05.100}{50}=0,1\left(mol\right)\)
- TH1: Axit dư
=> Tính theo số mol của rượu
\(n_{C_nH_{2n+1}OH}=a=n_{este\left(lý.thuyết\right)}=0,1\left(mol\right)\)
=> b = 0,2 (mol) (thỏa mãn)
(2) => 0,1n + 0,2m = 0,7 (**)
(*)(**) => n = 1; m = 3
=> CTPT: \(\left\{{}\begin{matrix}Rượu:CH_3OH\\Axit:C_3H_7COOH\end{matrix}\right.\)
- TH2: Rượu dư
=> Tính theo số mol axit
\(n_{CH_3COOH}=b=0,1\left(mol\right)\)
=> a = 0,2 (mol) (thỏa mãn)
(2) => 0,2n + 0,1m = 0,8 (***)
(*)(***) => n = 4; m = 0 (Vô lí)
- TH3: Pư vừa đủ
=> a = b (3)
(1)(3) => a = b = 0,15 (mol)
(2) => 0,15n + 0,15m = 0,75 (****)
(*)(****) => Vô nghiệm

CH 3 COOH + NaOH → CH 3 COONa + H 2 O
C n H 2 n + 1 COOH + NaOH → C n H 2 n + 1 COONa + H 2 O

nCO2 = 2,688/22,4 = 0,12 mol; nH2O = 2,52/18 = 0,14 mol
Ta thấy nH2O>nCO2 => ancol là ancol no, đơn chức, mạch hở
Gọi công thức chung của ancol là CkH2k+2O (k €N*)
Giả sử:
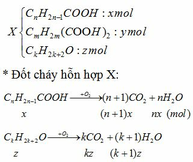
=> nH2O – nCO2 = nx – (n+1)x + (m+1)y – (m+2)y + (k+1)z – kz
=> 0,14 – 0,12 = -x - y + z hay -x - y + z = 0,02 (1)
BTNT ta tính được số mol của các nguyên tố:
nC = nCO2 = 0,12 mol
nH = 2nH2O = 2.0,14 = 0,28 mol
nO = 2nCnH2n-1COOH + 4nCmH2m(COOH)2 + nCkH2k+2O = 2x + 4y + z
=> mX = mC + mH + mO = 0,12.12 + 0,28.1 + 16(2x + 4y + z) = 32x + 64y + 16z + 1,72
* Phản ứng este hóa: Do sau phản ứng chỉ thu được chất có chứa chức este nên axit và ancol phản ứng vừa đủ
n ancol = x + 2y = z hay x + 2y – z = 0 (2)
BTKL ta có: mX = m este + mH2O => 32x + 64y + 16z + 1,72 = 3,22 + 18(x+2y)
hay 14x + 28y + 16z = 1,5 (3)
Từ (1) (2) (3) ta có hệ phương trình:
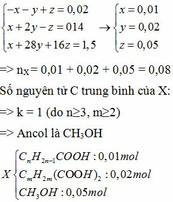
Bảo toàn nguyên tố C ta có: 0,01n + 0,02m + 0,05.1 = 0,12
=> n +2m = 7 mà do n≥3, m≥2 nên chỉ có cặp n = 3, m = 2 thỏa mãn
Vậy các axit trong X là: CH2=CH-COOH và HOOC-COOH.
Kết luận: Hỗn hợp X gồm các chất CH2=CH-COOH, HOOC-COOH và CH3OH.
- Một số ứng dụng của PVC trong thực tế như làm ống dẫn nước, vỏ dây điện, đồ giả da, áo mưa, nhãn chai nước khoáng, …