Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(2C_nH_{2n+1}COOH + 2Na \to 2C_nH_{2n+1}COONa + H_2\\ 2C_mH_{2m+1}OH + 2Na \to 2C_mH_{2m+1}ONa + H_2\\ C_nH_{2n+1}COOH + \dfrac{3n+1}{2}O_2 \xrightarrow{t^o} (n + 1)CO_2 + (n + 1)H_2O\\ C_mH_{2m+1}OH + \dfrac{3m}{2}O_2 \xrightarrow{t^o} m CO_2 + (m + 1)H_2O\\ C_nH_{2n+1}COOH + C_mH_{2m+1}OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons C_nH_{2n+1}COOC_mH_{2m+1} + H_2O\)
b)
Phần 1 :
n X + n Y = 2n H2 = 2.5,6/22,4 = 0,5(mol)
Phần 2 : n CO2 = 57,2/44 = 1,3(mol)
Phần 3 :
n X pư = n Y pư = n H2O = 2,7/18 = 0,15(mol)
- Nếu n X < n Y : Hiệu suất tính theo X
n X = 0,15/75% = 0,2(mol)
=> n Y = 0,5 - n X = 0,5 - 0,2 = 0,3 >n X = 0,2 ( thỏa mãn)
Bảo toàn nguyên tố với C :
(n + 1).n X + m.nY = n CO2
<=>(n + 1).0,2 + 0,3.m = 1,3
<=> 2n + 3m = 11
Với n = 1 ; m = 3 thì thỏa mãn . X là CH3COOH ; Y là C3H7OH
Với n = 4 ; m = 3 thì thỏa mãn . X là C4H9COOH ; Y là CH3OH
- Nếu n X > n Y : Hiệu suất tính theo Y
n Y = 0,15/75% = 0,2(mol)
=> n X = 0,5 - n Y = 0,5 - 0,2 = 0,3 > n Y(thỏa mãn)
n CO2 = (n + 1).n X + m.nY
<=>(n + 1)0,3 + 0,2.m = 1,3
<=> 3n + 2m = 10
Với n = 2 ; m = 2 thì thỏa mãn. X là C2H5COOH ; Y là C2H5OH

1)
- Xét phần 1:
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,2<-------------------0,2
=> nFe = 0,2 (mol)
- Xét phần 2:
\(n_{SO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
0,2-->0,6-------->0,1--------->0,3
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
0,3<----0,6<------0,3<-----0,3
=> nCu = 0,3 (mol)
m = 2.(0,2.56 + 0,3.64) = 60,8 (g)
2)
\(m_{H_2SO_4\left(bđ\right)}=\dfrac{200.98}{100}=196\left(g\right)\)
=> \(m_{H_2SO_4\left(sau.pư\right)}=196-98\left(0,6+0,6\right)=78,4\left(g\right)\)
mdd sau pư = \(\dfrac{60,8}{2}+200-0,6.64=192\left(g\right)\)
\(\left\{{}\begin{matrix}C\%_{\left(Fe_2\left(SO_4\right)_3\right)}=\dfrac{0,1.400}{192}.100\%=20,83\%\\C\%_{\left(CuSO_4\right)}=\dfrac{0,3.160}{192}.100\%=25\%\\C\%_{\left(H_2SO_4.dư\right)}=\dfrac{78,4}{192}.100\%=40,83\%\end{matrix}\right.\)

Đáp án A
Có
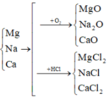
Vì các kim loại trong hỗn hợp X có hóa trị không đổi và khối lượng mỗi phần đều là 11 gam nên số mol electron trao đổi ở mỗi phần là như nhau.
Áp dụng định luật bảo toàn khối lượng ta có:
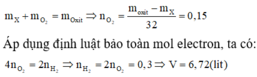


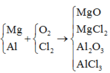
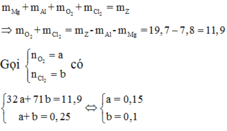
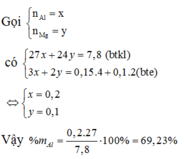
Gọi số mol của rượu, axit trong mỗi phần là a, b (mol)
- Phần 1:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: 2CnH2n+1OH + 2Na --> 2CnH2n+1ONa + H2
a---------------------------------->0,5a
2CmH2m+1COOH + 2Na --> 2CmH2m+1COONa + H2
b----------------------------------------->0,5b
=> 0,5a + 0,5b = 0,15 (1)
- Phần 2: \(n_{CO_2}=\dfrac{39,6}{44}=0,9\left(mol\right)\)
Bảo toàn C: an + b(m+1) = 0,9
=> an + bm + b = 0,9 (2)
- Phần 3:
PTHH: CnH2n+1OH + CmH2m+1COOH -H2SO4(đ),to-> CmH2m+1COOCnH2n+1 + H2O
Este có CTPT là Cm+n+1H2m+2n+2O2
=> m + n = 4 (*)
Ta có: \(n_{este\left(tt\right)}=\dfrac{5,1}{102}=0,05\left(mol\right)\)
Nếu hiệu suất là 100% => \(n_{este\left(lý.thuyết\right)}=\dfrac{0,05.100}{50}=0,1\left(mol\right)\)
- TH1: Axit dư
=> Tính theo số mol của rượu
\(n_{C_nH_{2n+1}OH}=a=n_{este\left(lý.thuyết\right)}=0,1\left(mol\right)\)
=> b = 0,2 (mol) (thỏa mãn)
(2) => 0,1n + 0,2m = 0,7 (**)
(*)(**) => n = 1; m = 3
=> CTPT: \(\left\{{}\begin{matrix}Rượu:CH_3OH\\Axit:C_3H_7COOH\end{matrix}\right.\)
- TH2: Rượu dư
=> Tính theo số mol axit
\(n_{CH_3COOH}=b=0,1\left(mol\right)\)
=> a = 0,2 (mol) (thỏa mãn)
(2) => 0,2n + 0,1m = 0,8 (***)
(*)(***) => n = 4; m = 0 (Vô lí)
- TH3: Pư vừa đủ
=> a = b (3)
(1)(3) => a = b = 0,15 (mol)
(2) => 0,15n + 0,15m = 0,75 (****)
(*)(****) => Vô nghiệm