Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(a.E_r=839,0+2\cdot418,4+2\cdot432,0=2539,8kJ\\ b.E_p=343,3+6\cdot418,4=2853,7kJ\\ c.\Delta_rH^{^{ }0}=2539,8-3197=-313,9kJ\cdot mol^{-1}\\ \Delta H< 0:pư.thu.nhiệt\)
\(a.E_{reactants}=839,0+2\cdot432,0=1703kJ\\ b.E_{products}=343,3+6\cdot432,0=2935,3kJ\\ c.\Delta_rH^{^o}_{298}=E_r-E_p=1703-2935,3=1232,3kJ\cdot mol^{^{ }-1}.\)
\(\Delta H< 0\) => Phản ứng (1) thu nhiệt

A đúng
B đúng, con người kiểm soát phản ứng phân hạch bằng lò phản ứng hạt nhân
D đúng, đặc biệt phản ứng nhiệt hạch không kèm theo tia phóng xạ, nên sạch hơn phân hạch.
C là đáp án sai.


ta có bảng về mối quan hệ giữa một kim loại với một số dung dịch muối:
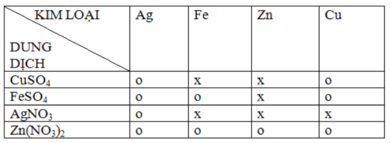
Viết các phương trình hóa học của phản ứng xảy ra theo dấu x
Fe + CuSO 4 → FeSO 4 + Cu
Zn + CuSO 4 → ZnSO 4 + Cu
Zn + FeSO 4 → ZnSO 4 + Fe
Fe + 2 AgNO 3 → Fe NO 3 2 + 2Ag
Zn + 2 AgNO 3 → Zn NO 3 2 + 2Ag
Cu + 2 AgNO 3 → Cu NO 3 2 + 2Ag

Đáp án C
1. Sai: cân bằng hóa học là cân bằng động
2. đúng: phản ứng nghịch thu nhiệt, khi tăng nhiệt độ cân bằng sẽ chuyển về phía làm giảm nhiệt độ (thu nhiệt).
3. đúng
4. đúng
5. sai, nồng độ thay đổi không làm thay đổi hằng số cân bằng. Hằng số cân bằng chỉ thay đổi khi thay đổi nhiệt độ.
6. sai: chỉ tính những chất khí hoặc những chất tan trong dung dịch, nếu là chất rắn thì không được tính.
=> Đáp án C