1. Cho các hỗn hợp, mỗi hỗn hợp gồm hai chất rắn có số mol bằng nhau: Na2O và Al2O3; Cu và Fe2(SO4)3; BaCl2 và Cu(NO3)2; Ba và NaHSO4; Al2O3 và Ba. Hỗn hợp nào tan hoàn toàn trong H2O (dư)? Giải thích
2. Cho 27,4 gam Ba vào 400 gam dung dịch CuSO4 3,2% thu được khí A, kết tủa B và dung dịch C.
a) Tính thể tích khí A (đktc)
b) Nung kết tủa B ở nhiệt độ cao đến khối lượng không đổi thì thu dược bao nhiêu gam chất rắn?
c) Tính nồng độ phần trăm của chất tan trong dung dịch C.

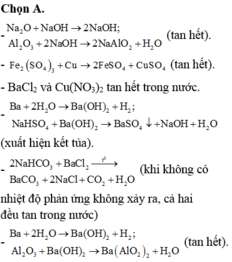
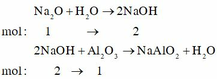
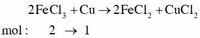
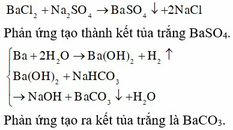


1. - Coi số mol từng chất trong các hỗn hợp đều bằng 1.
+ Na2O và Al2O3
PT: \(Na_2O+H_2O\rightarrow2NaOH\)
⇒ nNaOH = 2nNa2O = 0,2 (mol)
\(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\)
Xét tỉ lệ: \(\dfrac{1}{1}=\dfrac{2}{2}\), ta được pư vừa đủ.
→ Hỗn hợp tan hết
+ Cu và Fe2(SO4)3
PT: \(Cu+Fe_2\left(SO_4\right)_3\rightarrow CuSO_4+2FeSO_4\)
Xét tỉ lệ: \(\dfrac{1}{1}=\dfrac{1}{1}\), ta được pư vừa đủ
→ Hỗn hợp tan hết.
+ BaCl2 và Cu(NO3)2
→ Hỗn hợp tan hết trong nước vì 2 muối trên đều tan trong nước và không có pư với nhau.
+ Ba và NaHSO4.
PT: \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
⇒ nBa(OH)2 = nBa = 1 (mol)
\(Ba\left(OH\right)_2+2NaHSO_4\rightarrow BaSO_{4\downarrow}+Na_2SO_4+2H_2O\)
→ Hỗn hợp đầu tan hoàn toàn nhưng sau pư có xuất hiện kết tủa.
+ Al2O3 và Ba
PT: \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
⇒ nBa(OH)2 = nBa = 1 (mol)
\(Al_2O_3+Ba\left(OH\right)_2\rightarrow Ba\left(AlO_2\right)_2+H_2O\)
Xét tỉ lệ: \(\dfrac{1}{1}=\dfrac{1}{1}\), ta được pư vừa đủ.
→ Hỗn hợp tan hết
a, PT: \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
\(Ba\left(OH\right)_2+CuSO_4\rightarrow BaSO_{4\downarrow}+Cu\left(OH\right)_{2\downarrow}\)
\(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
Ta có: \(n_{Ba}=\dfrac{27,4}{137}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Ba}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, Ta có: \(n_{CuSO_4}=\dfrac{400.3,2\%}{160}=0,08\left(mol\right)\)
Theo PT: \(n_{Ba\left(OH\right)_2}=n_{Ba}=0,2\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,08}{1}\), ta được Ba(OH)2 dư.
Theo PT: \(n_{BaSO_4}=n_{Cu\left(OH\right)_2}=n_{CuO}=n_{Ba\left(OH\right)_2\left(pư\right)}=n_{CuSO_4}=0,08\left(mol\right)\)
⇒ m chất rắn = mBaSO4 + mCuO = 0,08.233 + 0,08.80 = 25,04 (g)
c, Ta có: m dd sau pư = mBa + m dd CuSO4 - mH2 - mBaSO4 - mCu(OH)2
= 27,4 + 400 - 0,2.2 - 0,08.233 - 0,08.98 = 400,52 (g)
nBa(OH)2 (dư) = 0,2 - 0,08 = 0,12 (mol)
\(\Rightarrow C\%_{Ba\left(OH\right)_2\left(dư\right)}=\dfrac{0,12.171}{400,52}.100\%\approx5,12\%\)