Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

Gọi số mol của BaO, BaCO3, NaHCO3 trong 30,19g hh lần lượt là x, y, z
Có 153x + 197y + 84z = 30,19
Phần 1:
BaO + H2O → Ba(OH)2
x x
OH- + HCO3- → CO32- + H2O
Ba2+ + CO32- → BaCO3
n kết tủa = 0,11
Phần 2:
BaCO3 →BaO + CO2
y y
2NaHCO3 → Na2CO3 + H2O + CO2
z z/2 z/2
=> mCO2 + mH2O = 30,19 – 26,13 = 4,06
=> 44 (y + z/2) + 18 . z/2= 4,06
TH1: Ba tạo kết tủa hoàn toàn thành BaCO3 và NaHCO3 dư
=> nBaCO3 = nBaCO3 + nBaO = 0,11 => Không thỏa mãn
TH2: Ba(OH)2 dư và NaHCO3 hết
=> x + y = 0,11 và y + z = 0,11
=> x = 0,1; y = 0,05 và z = 0,06
a.
hh Y gồm BaO: 0,15 mol; Na2CO3: 0,03 mol
BaO + H2O → Ba(OH)2
0,15 0,15
Ba(OH)2 + Na2CO3 → BaCO3 + 2NaOH
0,15 0,03 0,03 0,06
=> m kết tủa = 0,03 . 197 = 5,91g
m dd = m chất rắn + mH2O – mBaCO3 = 26,13 + 79,78 – 5,91 = 100
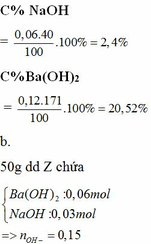
nAl2(SO4)3 = 0,02 => nAl3+ = 0,04; nSO42- = 0,06
Ba2+ + SO42- → BaSO4
0,06 0,06 0,06
nAl(OH)3 = 0,01 => mAl(OH)3 = 0,78g
m = 0,78 + 0,06 . 233 = 14,76g

Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
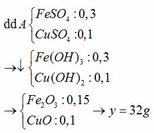





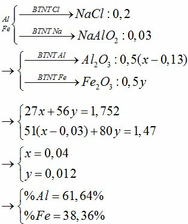



1. - Coi số mol từng chất trong các hỗn hợp đều bằng 1.
+ Na2O và Al2O3
PT: \(Na_2O+H_2O\rightarrow2NaOH\)
⇒ nNaOH = 2nNa2O = 0,2 (mol)
\(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\)
Xét tỉ lệ: \(\dfrac{1}{1}=\dfrac{2}{2}\), ta được pư vừa đủ.
→ Hỗn hợp tan hết
+ Cu và Fe2(SO4)3
PT: \(Cu+Fe_2\left(SO_4\right)_3\rightarrow CuSO_4+2FeSO_4\)
Xét tỉ lệ: \(\dfrac{1}{1}=\dfrac{1}{1}\), ta được pư vừa đủ
→ Hỗn hợp tan hết.
+ BaCl2 và Cu(NO3)2
→ Hỗn hợp tan hết trong nước vì 2 muối trên đều tan trong nước và không có pư với nhau.
+ Ba và NaHSO4.
PT: \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
⇒ nBa(OH)2 = nBa = 1 (mol)
\(Ba\left(OH\right)_2+2NaHSO_4\rightarrow BaSO_{4\downarrow}+Na_2SO_4+2H_2O\)
→ Hỗn hợp đầu tan hoàn toàn nhưng sau pư có xuất hiện kết tủa.
+ Al2O3 và Ba
PT: \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
⇒ nBa(OH)2 = nBa = 1 (mol)
\(Al_2O_3+Ba\left(OH\right)_2\rightarrow Ba\left(AlO_2\right)_2+H_2O\)
Xét tỉ lệ: \(\dfrac{1}{1}=\dfrac{1}{1}\), ta được pư vừa đủ.
→ Hỗn hợp tan hết
a, PT: \(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
\(Ba\left(OH\right)_2+CuSO_4\rightarrow BaSO_{4\downarrow}+Cu\left(OH\right)_{2\downarrow}\)
\(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
Ta có: \(n_{Ba}=\dfrac{27,4}{137}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Ba}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, Ta có: \(n_{CuSO_4}=\dfrac{400.3,2\%}{160}=0,08\left(mol\right)\)
Theo PT: \(n_{Ba\left(OH\right)_2}=n_{Ba}=0,2\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,08}{1}\), ta được Ba(OH)2 dư.
Theo PT: \(n_{BaSO_4}=n_{Cu\left(OH\right)_2}=n_{CuO}=n_{Ba\left(OH\right)_2\left(pư\right)}=n_{CuSO_4}=0,08\left(mol\right)\)
⇒ m chất rắn = mBaSO4 + mCuO = 0,08.233 + 0,08.80 = 25,04 (g)
c, Ta có: m dd sau pư = mBa + m dd CuSO4 - mH2 - mBaSO4 - mCu(OH)2
= 27,4 + 400 - 0,2.2 - 0,08.233 - 0,08.98 = 400,52 (g)
nBa(OH)2 (dư) = 0,2 - 0,08 = 0,12 (mol)
\(\Rightarrow C\%_{Ba\left(OH\right)_2\left(dư\right)}=\dfrac{0,12.171}{400,52}.100\%\approx5,12\%\)