Hòa tan hoàn toàn 57,6 gam kim loại Cu vào dd HNO3 loãng khí NO thu được đem oxi hóa thành NO2 rồi sục vào nước có dòng oxi để chuyển hết thành HNO3. Thể tích khí oxi ở đktc đã tham gia vào quá trình nên là bao nhiêu ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Các phản ứng xảy ra:
3Fe3O4 + 28HNO3 g 9Fe(NO3)3 + NO + 14H2O
NO + O2 g NO2
2NO2 + O2 + H2O g2HNO3
Trong toàn bộ quá trình, chỉ có nguyên tố Fe và O thay đổi số oxi hóa (nguyên tố N không có sự thay đổi số oxi hóa). Do đó ta có các quá trình nhường và nhận electron như sau:


Cách giải bài này nhanh nhất là dùng bảo toàn e ch ,nhận là ra ngay ,,mà thích pt thì có ::
3Cu+8HNO3 → 3Cu(NO3)2 + 2NO +4 H20
NO+1/2 O2 → NO2
NO2 +1/2O2 +1/2 H2O→ HNO3 Theo pt tính đk Vo2= 0,1.22,4= 2,24 l

Chọn đáp án C
+ Ta có: nHNO3 = 2nO/Oxit + 4nNO
⇔ nHNO3 pứ =
![]()
⇒ Chọn C

Đáp án : C
Bảo toàn khối lượng : mX + mO pứ = mY
=> nO pứ = nO (oxit) = 0,03 mol
Y + HNO3 -> nNO = 0,03 mol
Bảo toàn e :
ne KL = ne ( oxi) + ne(NO) = 0,03.2 + 0,03.3 = 0,15 mol
Mà ne KL = nNO3 muối = 0,15 mol
=> n H N O 3 = n N O 3 m u ố i + n N O
( Bảo toàn N ) = 0,15 + 0,03 = 0,18 mol

đáp án C
+ Ta có: nHNO3 = 2nO/Oxit + 4nNO
![]() nHNO3 pứ =
nHNO3 pứ = ![]() × 2 + 0,03 × 4 = 0,18 mol
× 2 + 0,03 × 4 = 0,18 mol
⇒ Chọn C

Đáp án B
Tổng quát: KL + Oxi → Oxit
=> Qui hỗn hợp Oxit thành dạng: KL, O
Bảo toàn khối lượng: mKL + mO = mOxit => mO = 2,71 – 2,23 = 0,48g
=> nO = 0,48: 16 = 0,03 mol
Khi Y + HNO3: nNO = 0,672: 22,4 = 0,03 mol
nHNO3 = 4nNO + 2nO = 4.0,03 + 2.0,03 = 0,18 mol





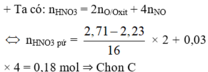

$n_{Cu} = \dfrac{57,6}{64} = 0,9(mol)$
$Cu^0 \to Cu^{+2} + 2e$
$O_2 + 4e \to 2O^{2-}$
Bảo toàn electron :$2n_{Cu} = 4n_{O_2}$
$\Rightarrow n_{O_2} = 1,8(mol)$
$V_{O_2} = 1,8.22,4 = 40,32(lít)$
A ơi a xem lại câu này đc k