Cho 20 gam hỗn hợp X( Al, Fe, Mg, Zn) đốt cháy trong khí Oxi dư thu được 28 gam các oxit Y. Hòa tan Y cần vừa đủ V ml dung dịch HCl 3M thu được dung dịch chứa m gam muối. Giá trị của V và m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn A
Bảo toàn khối lượng : mKL + mO = moxit => nO = 0,26 mol
Khi oxit phản ứng với HCl thì cũng tương tự như 1 mol O bị thay thế bởi 2 mol Cl-
=> nCl = 2nO = 0,52 mol
=> mKL + mCl = mmuối => m + 0,52.35,5 = 3m + 1,82
=> m = 8,32g
, mkết tủa = 9m + 4,06 = 78,94g
,nAgCl = nCl = 0,52 mol => Giả sử có Ag => nAg = 0,04 mol
Fe2+ + Ag+ -> Fe3+ + Ag
=> nFe2+ = nAg = 0,04 mol => nFeO(X) = 0,04
Vậy trong 3,75m (g) hỗn hợp X ( 31,2g) sẽ có nFeO = 0,04.31,2/(8,32 + 4,16) = 0,1
Khi phản ứng với HNO3 thì FeO -> Fe(NO3)3 ( Fe2+ -1e -> Fe3+)
Xét 3,75m gam X : Ta thấy nCl(muối) = ne trao đổi (1) = 1,3 mol
Khi phản ứng với HNO3 thì ne trao đổi (2) = ne trao đổi (1) + nFeO = nNO3 muối = 1,4 mol
=> m’ = mKL + mNO3 = 8,32.2,5 + 1,4.62 = 107,6g
( Nếu xét trường hợp không tạo NH4NO3)

Bảo toàn khối lượng :
\(m_{O_2}=3.43-2.15=1.28\left(g\right)\)
\(n_{O_2}=\dfrac{1.28}{32}=0.04\left(mol\right)\)
Bảo toàn O :
\(n_{H_2O}=2n_{O_2}=2\cdot0.04\cdot2=0.08\left(mol\right)\)
Bảo toàn H :
\(n_{HCl}=2n_{H_2O}=2\cdot0.08=0.16\left(mol\right)\)
\(V_{dd_{HCl}}=\dfrac{0.16}{0.5}=0.32\left(l\right)\)
Bảo toàn khối lượng :
\(m_{Muôi}=3.43+0.16\cdot36.5-0.08\cdot18=7.83\left(g\right)\)
Bảo toàn khối lượng:
m oxit = m kim loại + m O
=> mO = 3,43 – 2,15 = 1,28g
=> nO = 0,08 mol
Có nH+ = 2nO = 0,08 . 2 = 0,16 mol
V =\(\dfrac{0,16}{0,5}\)= 0,32 lít = 320ml
\(m_{muối}=m_{KL}+m_{Cl^-}=2,15+0,16.35,5=7,83\left(g\right)\)

Bảo toàn khối lượng :
\(m_{O_2}=44.6-28.6=16\left(g\right)\)
\(n_{O_2}=\dfrac{16}{32}=0.5\left(mol\right)\)
Bảo toàn O :
\(n_{H_2O}=2n_{O_2}=2\cdot0.5=1\left(mol\right)\)
Bảo toàn H :
\(n_{HCl}=2\cdot n_{H_2O}=2\cdot1=2\left(mol\right)\)
\(V_{dd_{HCl}}=\dfrac{2}{1}=2\left(l\right)\)
Bảo toàn khối lượng :
\(m_{Muối}=44.6+2\cdot36.5-1\cdot18=99.6\left(g\right)\)
\(n_O=\dfrac{44,6-28,6}{16}=1\left(mol\right)\)
\(n_{HCl}=n_{Cl^-}=n_O=2\left(mol\right)\)
\(m_{muối}=m_{KL}+m_{Cl^-}=28,6+2.35,5=99,6\left(g\right)\)
\(V_{HCl}=\dfrac{2}{1}=2\left(l\right)\)

Đáp án C
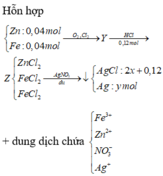
Khi tác dụng với HCl chỉ có các oxit bị hòa tan
→ nHCl = 4nO2 → nO2 = 0,03 mol
Gọi số mol của Cl2 và Ag lần lượt là x, y mol
Bảo toàn nguyên tố Cl → nAgCl = 2nCL2 + nHCl = 2. x + 0,12
→ 143,5( 2. x + 0,12) + 108y = 28,345
Bảo toàn electron cho toàn bộ quá trình 3nFe + 2nZn = 2nCl2 + 4nO2 + nAg
→ 3. 0,04 + 2.0,04 = 2.x + 4. 0,03 + y
Giải hệ → x= 0,035 và y = 0,01
![]()



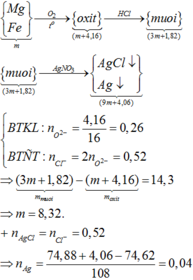

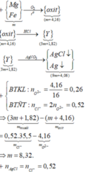
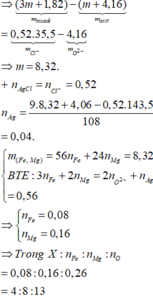
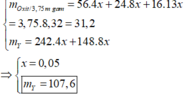
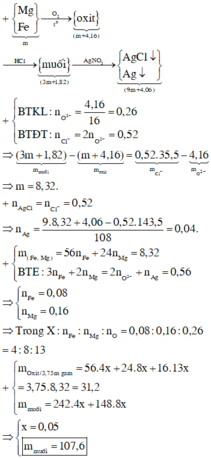
Coi hỗn hợp X là R có hoá trị n
$m_{O_2} = 28 - 20 = 8(gam) ; n_{O_2} = \dfrac{8}{32} = 0,25(mol)$
$4R + nO_2 \xrightarrow{t^o} 2R_2O_n$
$R_2O_n + 2nHCl \to 2RCl_n + nH_2O$
$n_{R_2O_n} = \dfrac{2}{n}n_{O_2} = \dfrac{0,5}{n}(mol)$
$n_{HCl} = 2n.n_{HCl} = 2n.\dfrac{0,5}{n} = 1(mol)$
$V = \dfrac{1}{3} = 0,33(lít) = 330(ml)$
$n_{H_2O} = \dfrac{1}{2}n_{HCl} = 0,5(mol)$
Bảo toàn khối lượng : $m = 28 + 1.36,5 - 0,5.18 = 55,5(gam)$
BTKL: \(m_{O_2}=m_Y-m_X=28-20=8\left(g\right)\)
\(n_{O_2}=\dfrac{8}{32}=0,25\left(mol\right)\)
Bảo toàn O: \(n_{H_2O}=2.n_{O_2}=0,25.2=0,5\left(mol\right)\)
Bảo toàn H: \(n_{HCl}=2.n_{H_2O}=2.0,5=1\left(mol\right)\)
\(V_{HCl}=\dfrac{1}{3}=0,33\left(l\right)\)
\(m_{H_2O}=0,5.18=9\left(g\right)\)
\(m_{HCl}=1.36,5=36,5\left(g\right)\)
BTKL: \(m_{muối}=m_Y+m_{HCl}-m_{H_2O}\)
\(=28+36,5-9=55,5\left(g\right)\)