Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A
Bảo toàn khối lượng : mKL + mO = moxit => nO = 0,26 mol
Khi oxit phản ứng với HCl thì cũng tương tự như 1 mol O bị thay thế bởi 2 mol Cl-
=> nCl = 2nO = 0,52 mol
=> mKL + mCl = mmuối => m + 0,52.35,5 = 3m + 1,82
=> m = 8,32g
, mkết tủa = 9m + 4,06 = 78,94g
,nAgCl = nCl = 0,52 mol => Giả sử có Ag => nAg = 0,04 mol
Fe2+ + Ag+ -> Fe3+ + Ag
=> nFe2+ = nAg = 0,04 mol => nFeO(X) = 0,04
Vậy trong 3,75m (g) hỗn hợp X ( 31,2g) sẽ có nFeO = 0,04.31,2/(8,32 + 4,16) = 0,1
Khi phản ứng với HNO3 thì FeO -> Fe(NO3)3 ( Fe2+ -1e -> Fe3+)
Xét 3,75m gam X : Ta thấy nCl(muối) = ne trao đổi (1) = 1,3 mol
Khi phản ứng với HNO3 thì ne trao đổi (2) = ne trao đổi (1) + nFeO = nNO3 muối = 1,4 mol
=> m’ = mKL + mNO3 = 8,32.2,5 + 1,4.62 = 107,6g
( Nếu xét trường hợp không tạo NH4NO3)

Mol \(Fe\) = 0,11 mol
Mol hh khí= 0,1 mol
BT klg\(\Rightarrow\)m hh khí=12,09-6,16=5,93g
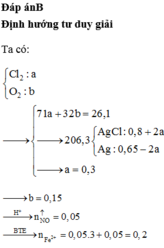
Gọi mol \(Cl_2\) và mol \(O_2\) lần lượt là x và y
\(\Rightarrow\) x+y=0,1 và 71x+32y=5,93
\(\Rightarrow\)x=0,07 và y=0,03
Mol \(Cl-\) trong muối= 0,07.2=0,14 mol = mol \(AgCl\)
\(Fe\) có thể lên \(Fe+2\) và \(Fe+3\) nên
\(Fe\Rightarrow Fe^{+2}+2e\)
a mol. \(\Rightarrow\)2a mol
\(Fe\Rightarrow Fe^{+3}+3e\)
b mol \(\Rightarrow\)3b mol
\(Cl_2+2e\Rightarrow2Cl-\)
0,07 \(\Rightarrow\)0,14 mol
\(O_2+4e\Rightarrow2O_2-\)
0,03\(\Rightarrow\)0,12 mol
Mol e nhường= nhận\(\Rightarrow\)2a+3b=0,26 mol và tổng mol \(Fe\)là a+b=0,11 mol\(\Rightarrow\)a=0,07 và b=0,04
\(Fe^{2+}+Ag^+\Rightarrow Fe^{3+}+Ag\)
0,07 mol \(\Rightarrow\)0,07 mol
Số gam kết tủa = 0,07.108+0,14.143,5=27,65\(\Rightarrow\)chọn A
Đáp án b nhé :44,87...lưu ý khi tính ra số mol fe2+ = 0,07, mol fe3+=0,04 thì =>>> mol Cl- = 0,07x2 + 0,04x3= 0,26 mol.....==>> mol AgCl=0,26.......Để ý hòa tan bằng dd Hcl vừa đủ thì oxit phải chuyển thành hết muối clorua....ko đẻ ý điều này rất dễ nhầm đáp án là A...lừa đó ^^

Ta có sơ đồ phản ứng:
m(gam) (Mg, Fe) + --O2→ (m+4,16) gam B + --HCl→ D (Mg2+ x mol; Fe2+ y mol; Fe3+ z mol); Cl-)
D + --AgNO3→ (11m – 12,58) gam (Ag + AgCl)
Ta có m(O) = 4,16 gam → n(O) = 0,26 mol → n(Cl- trong D) = 0,52 mol
→ n(AgCl) = 0,52 mol
Ta có hệ phương trình
(1): 24x + 56(y+z) = m
(2) ĐLBT điện tích: 2x+2y+ 3z = 0,52
(3) m + 0,52*35,5 = 4m-6,5
→ m = 8,32 gam → n(Ag) = 0,04 = y → x = 0,16; z = 0,04
Mặt khác trong 4,5m gam A có: Mg = 0,72 mol và Fe 0,36 mol
Dung dịch muối: Mg2+: 0,72 mol; Fe3+: 0,36mol; NH4+: t mol; NO3-: q mol
hợp khí F gồm N2 (0,04 mol) và N2O (0,04 mol)
Áp dụng ĐLBT mol e: → t = 0,225 mol
Áp dụng ĐLBT điện tích → q = 2,745 mol → m 211,68 gam → Đáp án C

Đáp án C.
→ B T K L n O = 4 , 16 16 = 0 , 26 → n C l - = 0 , 52 → m + 0 , 52 . 35 , 5 = 4 m - 6 , 5 → m = 8 , 32 m k t = 78 , 94 ; n A g C l = 0 , 52 → n A g = 0 , 04 → B T e n e = 0 , 26 . 2 + 0 , 05 = 0 , 56 → n N 2 = n N 2 O = 0 , 04 → B T e n N H 4 N O 3 = 0 , 56 . 4 , 5 - 0 , 04 . 10 - 0 , 04 . 10 8 = 0 , 225 → a = 0 , 225 . 80 + 8 , 32 . 4 , 5 + 0 , 56 . 4 , 5 . 62 = 211 , 68

Đáp án B
Có m h h k h í = 6,11; n h h k h í = 0,13
=> n C l 2 = 0,05; n O 2 = 0,08.
Hòa tan hết Y trong HCl nên có: n H C l = 2. n H 2 O = 2. n O 2 - = 0,32 mol
- BTNT (Cl):
n C l - t r o n g Z = n A g C l = n H C l + n C l - = 0,32 + 0,1 = 0,42. → m A g C l = 0,42.143,5 = 60,27 gam
→ m k ế t t ủ a = m A g C l + m A g → m A g = 73,23 – 60,27 = 12,96 → n A g = 0,12 mol.
=> n F e 2 + = 0,12.
BTĐT trong Z: 2.0,12 + 2. n C u = 0,42 => n C u = 0,09.
Vậy X chứa Fe (0,12) và Cu(0,09).
Khi X tác dụng HNO3, ta thấy: (0,12 × 3 + 0,09 × 2) ÷ 3 = 0,18 mol > n N O = 0,15 mol
có nghĩa là Fe không lên hết Fe3+ mà có 1 phần chỉ lên Fe2+
Khi phản ứng với HNO3: nFe(III) = a mol ; nFe(II) = bmol. ta có hệ:
a + b = 0,12
3a + 2b + 0,09.2 = 0,15.3
Giải hệ: a = 0,03; b = 0,09.
Vì HNO3 dùng hết, n H N O 3 = 4 n N O = 0,6 mol → m H N O 3 = 37,8 → m d d H N O 3 = 120 gam.
→ BTKL: m d d T = m X + m H N O 3 - m N O = 127,98 gam.
% C F e ( N O 3 ) 3 t r o n g T = 0,03 . 242 : 127,98 ≈ 5,67%.
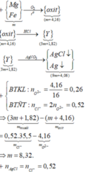
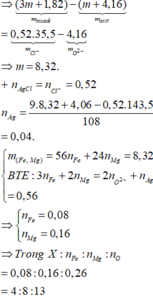
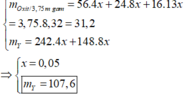

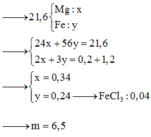
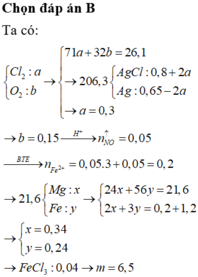
Đáp án D