Một mẫu quặng chứa 82% Fe2O3 . phần trăm khối lượng của chất sắt trong quặng là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

một loại quặng chứa 82% Fe2O3. Thành phần phần trăm của Fe trong quặng theo khối lượng là bao nhiêu?


Phương trình hóa học:
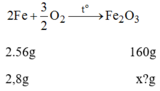
Khối lượng F e 2 O 3 ứng với lượng sắt trên là:
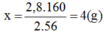
→ Chọn C.

a. nH2 = nFe = 0,1mol
Bảo toàn nguyên tố Fe => nFe2O3 = 0,05mol
=> mFe2O3 = 8g
=> %Fe2O3 = (8:10) . 100% = 80%

Ta có: \(\dfrac{m_M}{m_N}=\dfrac{2}{5}\Rightarrow5m_M-2m_N=0\left(1\right)\)
Mà: mM + mN = 1 (tấn) = 1000 (kg) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}m_M=\dfrac{2000}{7}\left(kg\right)\\m_N=\dfrac{5000}{7}\left(kg\right)\end{matrix}\right.\)
\(\Rightarrow m_{Fe_2O_3}=m_M.60\%=\dfrac{1200}{7}\left(kg\right)\Rightarrow n_{Fe_2O_3}=\dfrac{\dfrac{1200}{7}}{160}=\dfrac{15}{14}\left(kmol\right)\)
\(\Rightarrow n_{Fe}=2n_{Fe_2O_3}=\dfrac{15}{7}\left(kmol\right)\)
\(m_{Fe_3O_4}=m_N.69,6\%=\dfrac{3480}{7}\left(kg\right)\Rightarrow n_{Fe_3O_4}=\dfrac{\dfrac{3480}{7}}{232}=\dfrac{15}{7}\left(kmol\right)\)
\(\Rightarrow n_{Fe}=3n_{Fe_3O_4}=\dfrac{45}{7}\left(kmol\right)\)
\(\Rightarrow m_{Fe}=\left(\dfrac{15}{7}+\dfrac{45}{7}\right).56=480\left(kg\right)\)

Bạn xem lời giải ở đây nhé.
https://olm.vn/hoi-dap/detail/7712766586263.html

coi $m_{quặng} = 100(gam)$
$m_{Fe_2O_3} = 100.82\% = 82(gam)$
$n_{Fe_2O_3} = \dfrac{82}{160} = 0,5125(mol)$
$n_{Fe} = 2n_{Fe_2O_3} = 1,025(mol)$
$\%m_{Fe} = \dfrac{1,025.56}{100}.100\% = 57,4\%$