Hòa tan hoàn toàn 3,84 gam Cu trong dung dịch HNO3 dư, thu được hỗn hợp khí NO (sản phẩm khử duy nhất). Trộn một lượng NO trên với O2 dư thu được hỗn hợp khí Y. Sục khí Y vào nước dư, thu được dung dịch Z, và còn lại khí O2 duy nhất. Tổng thể tích O2 (đktc) đã phản ứng là :
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

2 tháng 11 2019
Đáp án : B
Gọi sốm ol NO và NO2 lần lượt là x và y mol
Bảo toàn e : 2nCu = 3x + y = 0,12 mol
Lại có : NO + ½ O2 à NO2
4NO2 + O2 + 2H2O à 4HNO3
=> nO2 pứ = 3 x + y 4 = V - 0 , 25 V 22 , 4
=> V = 0,896 lít

24 tháng 6 2017
Đáp án B
- Khi cho hỗn hợp tác dụng với H2SO4 loãng dư chỉ có Mg phản ứng sinh ra khí H2 => nMg=nH2=0,15 mol
- Khi cho hỗn hợp tác dụng với HNO3 dư => Chỉ có Cu và Mg (kim loại thay đổi số oxi hóa)
BT e: nCu=(3nNO-2nMg)/2=0,15 mol
=>mCu=0,15.64=9,6 gam
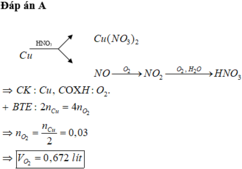







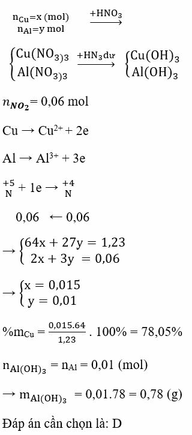
$n_{Cu} = \dfrac{3,84}{64} = 0,06(mol)$
Bảo toàn electron :
$Cu^0 \to Cu^{+2} + 2e$
$O_2 + 4e \to 2O^{-2}$
Bảo toàn electron : $2n_{Cu} = 4n_{O_2} \Rightarrow n_{O_2} = \dfrac{1}{2}n_{Cu} = 0,03(mol)$
$V_{O_2\ pư} = 0,03.22,4 = 0,672(lít)$
$n_{Cu} = \dfrac{3,84}{64} = 0,06(mol)$
Bảo toàn electron :
$Cu^0 \to Cu^{+2} + 2e$
$O_2 + 4e \to 2O^{-2}$
Bảo toàn electron : $2n_{Cu} = 4n_{O_2} \Rightarrow n_{O_2} = 2n_{Cu} = 0,12(mol)$
$V_{O_2\ pư} = 0,12.22,4 = 2,688(lít)$