Cho 1.67 gam hỗn hợp 2 kim loại ở 2 chu kì liên tiếp thuộc nhóm IIA(phân nhóm chính nhóm IIA)tác dụng hết với dung dịch HCl(dư) , thoát ra 0.672lit khí H2(ở dktc) . Hai kim loại đó là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B.
Gọi công thức chung của hai kim loại là X
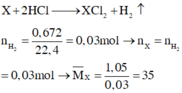
Mà hai kim loại ở 2 chu kỳ liên tiếp thuộc nhóm IIA → 2 kim loại đó là Ca và Mg

Đáp án B.
Gọi công thức chung của hai kim loại là X
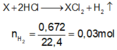
![]()
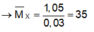
Mà hai kim loại ở 2 chu kỳ liên tiếp thuộc nhóm IIA → 2 kim loại đó là Ca và Mg

Đáp án A
Kim loại nhóm IIA, có mức oxi hóa = +2 trong hợp chất
nH2 = 0,03 mol
Gọi X là kí hiệu chung của 2 kim loại
X + 2HCl → XCl2 + H2
0,03 ← 0,03 (mol)
⇒ M = 55,6
MCa = 40 < 55,67 < MSr = 88

Vì hai kim loại đều thuộc nhóm IIA nên đặt công thức chung của hỗn hợp kim loại là là X ¯ ( X ¯ có hóa trị II không đổi).
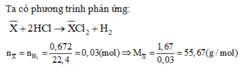
Do đó trong hỗn hợp có 1 kim loại có khối lượng mol nhỏ hơn 55,67 và 1 kim loại có khối lượng mol lớn hơn 55,67.
Mặt khác hai kim loại này thuộc hai chu kì liên tiếp.
Nên 2 kim loại cần tìm là Ca và Sr.
Đáp án D.






\(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
Gọi công thức chung 2 kim loại là R
PTHH: \(R+2HCl\rightarrow RCl_2+H_2\)
0,03<------------------0,03
=> \(M_R=\dfrac{1,67}{0,03}=55,67\left(g/mol\right)\)
Mà 2 kim laoij ở 2 chu kì liên tiếp nhóm IIA
=> 2 kim loại là Ca, Sr
Gọi CT chung của 2 kim loại là R
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
PTHH: R + 2HCl ---> RCl2 + H2
0,03<------------------0,03
=> \(M_R=\dfrac{1,67}{0,03}=\dfrac{167}{3}\) (g/mol)
Mà 2 kim loại này thuộc chu kì liên tiếp nhau trong nhóm IIA trong bảng tuần hoàn => 2 kim loại này là Ca và Sr