Nung hỗn hợp X gồm a (mol) FeS và b (mol) FeS2 trong một bình kín chứa không khí (gồm 20% thể tích O2 và 80% thể tích N2) đến khi các phản ứng xảy ra hoàn toàn, thu được một chất rắn duy nhất và hỗn hợp khí Y có thành phần thể tích 84,8% N2, 14% SO2, còn lại là O2. Tính tỉ lệ a/b. Giúp tớ với ạa
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn C
N 2 : 0 , 848 m o l S O 2 : 0 , 14 m o l O 2 d u : 1 − 0 , 848 − 0 , 14 = 0 , 012 m o l → K h ô n g k h í N 2 : 0 , 848 m o l O 2 : 0 , 212 m o l
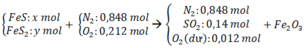
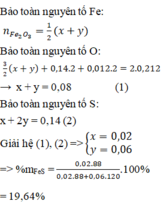

Chọn 1 mol hỗn hợp Y =>số mol N2 = 0,848 mol; số mol O2 ban đầu = 0,212 mol
=>số mol O2 phản ứng = 0,212 – 0,012 = 0,2 mol
2FeS + 3,5O2 → Fe2O3 + 2SO2
a→ 1,75a→ a
2FeS2 + 5,5O2 → Fe2O3 + 4SO2
b → 2,75b → 2b
=>1,75a+2,75b = 0,2
a+2b= 0,14
=>a=0,02; b=0,06
%khối lượng FeS = 0,02.88\0,02.88+0,06.120.100% = 19,64%

Đáp án : B
Xét 1 mol không khí : 0,2 mol O2 và 0,8 mol N2
%nN2 = 84,77% => nY = 0,94373 mol
=> nSO2 = 0,1 mol
,nO2 dư = 0,0437 mol
=> nO2 pứ = 0,2 – 0,044 = 0,1563 mol
2FeS + 3,5O2 -> Fe2O3 + 2SO2
.a -> 1,75a
2FeS2 + 5,5O2 -> Fe2O3 + 4SO2
.b -> 2,75b
=> ¼ (7a + 11b) = 0,1563
.a + 2b = 0,1
=> a = 0,05 mol ; b = 0,025 mol
=> mX = 7,4g
=> %mFeS = 59,46%

Đáp án A
Chọn 100 mol không khí.
Tỉ lệ thể tích cũng là tỉ lệ số mol nên
![]()
Gọi 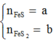
Có
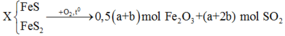

![]()
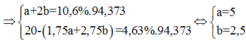
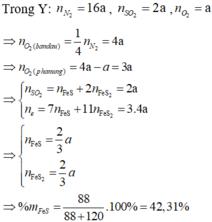
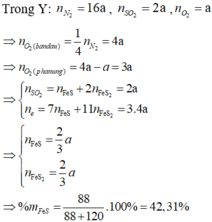
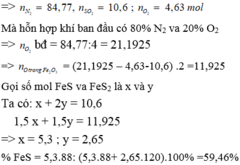
PTHH: \(4FeS+7O_2\underrightarrow{t^o}2Fe_2O_3+4SO_2\)
a--->1,75a------------>a
\(4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\)
b---->2,75b------------->2b
=> \(\left\{{}\begin{matrix}n_{SO_2}=a+2b\left(mol\right)\\n_{O_2\left(pư\right)}=1,75a+2,75b\left(mol\right)\end{matrix}\right.\)
Giả sử có x mol không khí
=> \(\left\{{}\begin{matrix}n_{O_2\left(bđ\right)}=0,2x\left(mol\right)\\n_{N_2}=0,8x\left(mol\right)\end{matrix}\right.\)
\(n_Y=\dfrac{\left(a+2b\right).100}{14}=\dfrac{50}{7}a+\dfrac{100}{7}b\left(mol\right)\)
Ta có: \(\%V_{N_2}=\dfrac{0,8x}{\dfrac{50}{7}a+\dfrac{100}{7}b}.100\%=84,8\%\)
=> \(x=\dfrac{53}{7}a+\dfrac{106}{7}b\left(mol\right)\) (1)
Ta có: \(0,8x+\left(0,2x-1,75a-2,75b\right)+a+2b=\dfrac{50}{7}a+\dfrac{100}{7}b\)
=> \(x=\dfrac{221}{28}a+\dfrac{421}{28}b\left(mol\right)\) (2)
(1)(2) => \(\dfrac{9}{28}a=\dfrac{3}{28}b\) => a : b = 1 : 3
Giả sử có 1 mol hỗn hợp khí có:
\(\left\{{}\begin{matrix}n_{N_2}=0,848\left(mol\right)\\n_{SO_2}=0,14\left(mol\right)\\n_{O_2\left(dư\right)}=1-0,848-0,14=0,012\left(mol\right)\end{matrix}\right.\)
\(n_{kk}=\dfrac{0,848}{80\%}=1,06\left(mol\right)\\ \rightarrow n_{O_2\left(pư\right)}=1,06-0,012-0,848=0,2\left(mol\right)\)
PTHH:
\(4FeS+7O_2\xrightarrow[]{t^o}2Fe_2O_3+4SO_2\)
a------>1,75a--------------->a
\(4FeS_2+11O_2\xrightarrow[]{t^o}2Fe_2O_3+8SO_2\)
b-------->2,75b------------------>2b
=> \(\left\{{}\begin{matrix}1,75a+2,75b=0,2\\a+2b=0,14\end{matrix}\right.\)
=> a = 0,02; b = 0,06
\(\dfrac{a}{b}=\dfrac{0,02}{0,06}=\dfrac{1}{3}\)