Câu 1 : nhận biết HCL, NaOH , H2SO4
Câu 2 : cho 4,8 gam MgSO3 kim loại magie tác dụng vừa đủ với dd axit sunfuric , thể tích khí Hidro thu đc ở đktc là :
A . 44,8 lít ; B. 4,48 lít ; C. 2,24 lít ; D 22,4 lít
câu 3 : cho 0,1 mol kim loại kẽm vào dd HCL dư . khối lượng muối thu đc là
A . 13,6g B . 1,36g C. 20,4 g D. 27,2g
câu 4 : cho 21g MgCO3 tác dụng với một lượng vừa đủ dd HCL 2M
A . 2,5 lít B . 0,25 lít C. 3,5 lít D. 1,5 lít
Câu 5 : hòa tan 16 gam SO3 trong nược thu đc 250 ml dd axit . nồng độ mol dd axit thu đc là :
A. CM(H2SO4)= 0,2 M B. CM(H2SO4)= 0,4 M C.CM(H2SO4)= 0,6 M
* viết các phương trình xảy ra
H2 + Cl2 -->
HCl + AgNO3 -->
NaCl + AgNO3 -->
Cl12H22O11 (H2SO4)--->
H2SO4 + BaCl2 ------>
NA2SO4 + BaCl2 -->

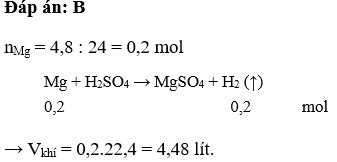
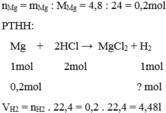
Câu 1:
- Trích một ít các dd làm mẫu thử
- Cho các dd tác dụng với giấy quỳ tím:
+ Qt chuyển xanh: NaOH
+ Qt chuyển đỏ: H2SO4, HCl (1)
- Cho dd ở (1) tác dụng với dd BaCl2:
+ Không hiện tượng: HCl
+ Kết tủa trắng: H2SO4
\(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
Câu 2: B
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
0,2------------------------>0,2
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
Câu 3: A
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1-------------->0,1
\(\Rightarrow m_{ZnCl_2}=0,1.136=13,6\left(g\right)\)
Câu 4:
Đề hỏi thể tích dd HCl đúng không nhỉ ?
\(n_{MgCO_3}=\dfrac{21}{84}=0,25\left(mol\right)\)
PTHH: \(MgCO_3+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
0,25----->0,5
\(\Rightarrow V_{dd.HCl}=\dfrac{0,5}{2}=0,25\left(l\right)\)
=> B
Câu 5:
\(n_{SO_3}=\dfrac{16}{80}=0,2\left(mol\right)\)
PTHH: \(SO_3+H_2O\rightarrow H_2SO_4\)
0,2-------------->0,2
\(\Rightarrow C_{M\left(dd.H_2SO_4\right)}=\dfrac{0,2}{0,25}=0,8M\)
(bn check lại phần đáp án nhé :))
*
\(H_2+Cl_2\underrightarrow{as}2HCl\)
\(HCl+AgNO_3\rightarrow AgCl\downarrow+HNO_3\)
\(NaCl+AgNO_3\rightarrow AgCl\downarrow+HNO_3\)
\(C_{12}H_{22}O_{11}\underrightarrow{H_2SO_4}12C+11H_2O\)
\(H_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2HCl\)
\(Na_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2NaCl\)
Câu 2 : cho 4,8 gam MgSO3 kim loại magie tác dụng vừa đủ với dd axit sunfuric , thể tích khí Hidro thu đc ở đktc là :
A . 44,8 lít ; B. 4,48 lít ; C. 2,24 lít ; D 22,4 lít
câu 3 : cho 0,1 mol kim loại kẽm vào dd HCL dư . khối lượng muối thu đc là
A . 13,6g B . 1,36g C. 20,4 g D. 27,2g
câu 4 : cho 21g MgCO3 tác dụng với một lượng vừa đủ dd HCL 2M
A . 2,5 lít B . 0,25 lít C. 3,5 lít D. 1,5 lít