Mọi người giúp mình bài 2 với ạ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(R_{tđ}=\dfrac{R_1\cdot R_2}{R_1+R_2}=\dfrac{24\cdot12}{24+12}=8\Omega\)
\(I=\dfrac{U}{R}=\dfrac{12}{8}=1,5A\)
\(P=\dfrac{U^2}{R}=\dfrac{12^2}{8}=18W\)
\(Q_{tỏa1}=A_1=U_1\cdot I_1\cdot t=12\cdot\dfrac{12}{24}\cdot1\cdot3600=21600J\)
\(Q_{tỏa2}=A_2=U_2\cdot I_2\cdot t=12\cdot\dfrac{12}{12}\cdot1\cdot3600=43200J\)

Bài 1:
Vì (d)//y=-2x+1 nên a=-2
Vậy: y=-2x+b
Thay x=1 và y=2 vào (d),ta được:
b-2=2
hay b=4

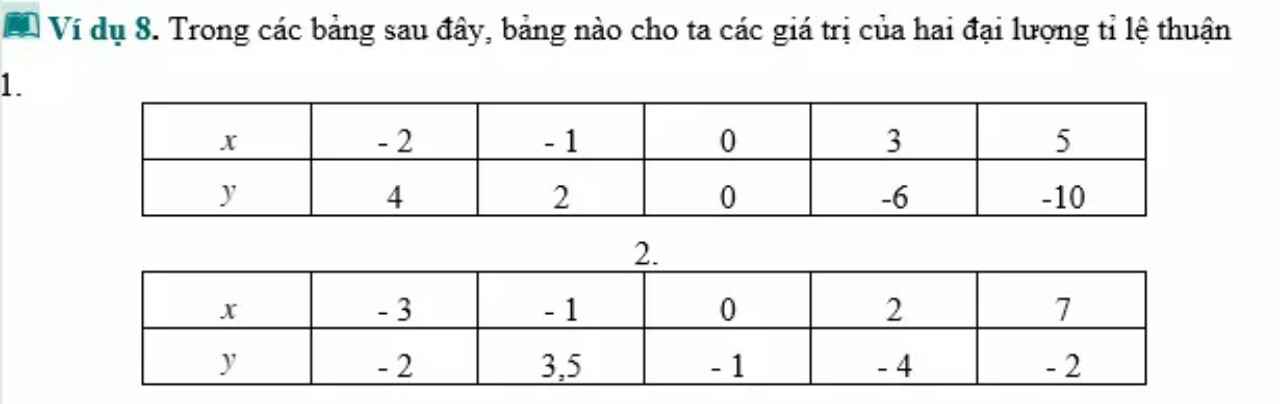
đề hỏi là xác định bảng nào là đại lượng tỉ lệ thuận mà chứ có kêu tìm gì đâu bạn

Mình đang càn gấp câu c ạ, mọi người giúp mình câu c được không ạ??
Gọi nMg=x mol, nAl=y mol
nH2=\(\dfrac{5,6}{22,4}=0,25mol\)
Mg + 2HCl → MgCl2 + H2
x → 2x → x → x
2Al + 6HCl → 2AlCl3 + 3H2
y → 3y → y → 1,5y
\(\left\{{}\begin{matrix}24x+27y=5,1\\x+1,5y=0,25\end{matrix}\right.\) ⇔ \(\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
a) %Mg=\(\dfrac{0,1.24}{5,1}.100\%\approx47,06\%\)
%Al = 100% - 47,06%=52,94%
b) nHCl=2x+3y=0,1.2+0,1.3=0,5 mol
mHCl = 0,5 . 36,5=18,25g
m=\(\dfrac{18,25.100}{10}=182,5g\)
c) MgCl2 + 2NaOH → Mg(OH)2 + 2NaCl
x → x
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
y → y
a = mMg(OH)2 + mAl(OH)3
= 0,1.58 + 0,1.78 =13,6g

b) Đặt (d3): y=ax+b
Vì (d3)//(d1) nên \(a=-\dfrac{2}{3}\)
Vậy: (d3): \(y=\dfrac{-2}{3}x+b\)
Thay x=6 vào (d2), ta được:
\(y=-2\cdot6+4=-12+4=-8\)
Thay x=6 và y=-8 vào (d3), ta được:
\(\dfrac{-2}{3}\cdot6+b=-8\)
\(\Leftrightarrow b=-4\)
Vậy: (d3): \(y=\dfrac{-2}{3}x-4\)

Bài 1:
(1) \(4Al+3O_2\xrightarrow[]{t^o}2Al_2O_3\)
(2) \(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
(3) \(AlCl_3+3KOH\rightarrow3KCl+Al\left(OH\right)_3\downarrow\)
(4) \(Al\left(OH\right)_3+3HCl\rightarrow AlCl_3+3H_2O\)
(5) \(2Al\left(OH\right)_3\xrightarrow[]{t^o}Al_2O_3+3H_2O\)
(6) \(Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+2H_2O\)
(7) \(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\)
(8) \(Al+NaOH+H_2O\rightarrow NaAlO_2+\dfrac{3}{2}H_2\uparrow\)
(9) \(2Al_2O_3\xrightarrow[criolit]{đpnc}4Al+3O_2\)
Bài 2:
PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
a_______a_______a_____a (mol)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
b_______b________b____b (mol)
Ta lập HPT: \(\left\{{}\begin{matrix}56a+24b=21,6\\a+b=\dfrac{11,2}{22,4}=0,5\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,3\\b=0,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,3\cdot56}{21,6}\cdot100\%\approx77,78\%\\\%m_{Mg}=22,22\%\end{matrix}\right.\)
Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_{Mg\left(OH\right)_2}=n_{Mg}=0,2\left(mol\right)\\n_{Fe\left(OH\right)_2}=n_{Fe}=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{kết.tủa}=m_{Fe\left(OH\right)_3}+m_{Mg\left(OH\right)_2}=0,3\cdot107+0,2\cdot56=43,3\left(g\right)\)
Theo các PTHH: \(n_{H_2SO_4\left(p/ứ\right)}=0,5\left(mol\right)\) \(\Rightarrow n_{H_2SO_4\left(ban.đầu\right)}=0,5\cdot120\%=0,6\left(mol\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,6\cdot98}{10\%}=588\left(g\right)\)
Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_{MgO}=n_{Mg}=0,2\left(mol\right)\\n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{chất.rắn}=m_{MgO}+m_{Fe_2O_3}=0,2\cdot40+0,15\cdot160=32\left(g\right)\)

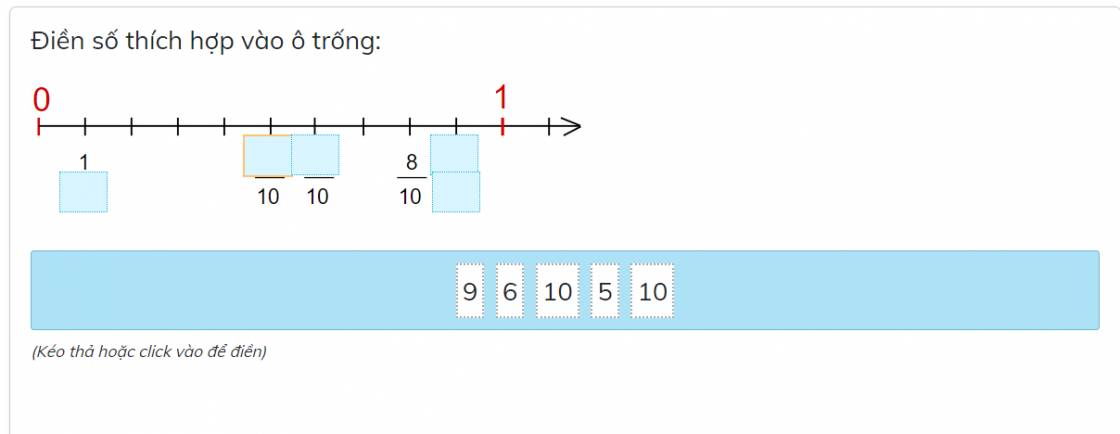
Từ 0 đến 1 được chia thành 10 phần bằng nhau.
Giá trị của mỗi phần là: \(\dfrac{1}{10}\)
Từ lập luận trên ta có:
Số thích hợp để điền vào các ô trống lần lượt là:
10; 5; 6; 9; 10
0 ; 1/10 ; 2/10 ; 3/10 ; 4/10 ; 5/10 ; 6/10 ; 7/10 ; 8/10 ; 9/10 ; 1
Chúc bạn học tốt!







Bài 2:
a: Thay x=-1 và y=1 vào \(y=ax^2\), ta được:
\(a\cdot\left(-1\right)^2=1\)
hay a=1
b: Vì (d): y=ax+b có hệ số góc là 1 nên a=1
Vậy: (d): y=x+b
Thay x=-1 và y=1 vào (d), ta được:
b-1=1
hay b=2
Vậy: (d): y=x+2
Phương trình hoành độ giao điểm là:
\(x^2-x-2=0\)
=>(x-2)(x+1)=0
=>x=2 hoặc x=-1
Khi x=2 thì y=4
Khi x=-1 thì y=1
Vậy: B(2;4)