Câu 12: Cho 23g Na vào trong 100g nước. Tính C% của dung dịch sau khi Na tan hết
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Giải thích:
nNa = 23: 23 = 1 (mol)
2Na + 2H2O → 2NaOH + H2↑
1 →1 → 0,5
mdd sau = mNa + mH2O – mH2 = 23 + 100- 0,5.2 = 122g
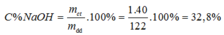
Đáp án C

a) mdd =15+65=80g
b)
⇒SNa2CO3=\(\dfrac{53}{250}\).100=21,2g
Vậy độ tan của muối Natricacbonat ở 18 độ C là 21,2g
a. mdd = 15+65 = 80 (g)
b. Độ tan của muối Na2CO3 ở 18^oC là : S = (53 x 100)/250 = 21,2 (gam).

a) PTHH: \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\)
b) Ta có: \(n_{Na}=\dfrac{2,3}{23}=0,1\left(mol\right)=n_{NaOH}\) \(\Rightarrow m_{NaOH}=0,1\cdot40=4\left(g\right)\)
c) PTHH: \(H_2+CuO\xrightarrow[]{t^o}Cu+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{H_2}=0,05\left(mol\right)\\n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) CuO còn dư, Hidro p/ứ hết
\(\Rightarrow\left\{{}\begin{matrix}n_{Cu}=0,05\left(mol\right)\\n_{CuO\left(dư\right)}=0,075\left(mol\right)\end{matrix}\right.\) \(\Rightarrow m_{rắn}=m_{Cu}+m_{CuO}=9,2\left(g\right)\)

mH2O = 47,8 . 1 = 47,8 (g)
nH2O = 47,8/18
nNa = 2,3/23 = 0,1 (mol)
PTHH: 2Na + 2H2O -> 2NaOH + H2
0,1 ---> 0,1 ---> 0,1 ---> 0,05
mNaOH = 0,1 . 40 = 4 (g)
mH2 = 0,05 . 2 = 0,1 (g)
mdd (sau p/ư) = 47,8 + 2,3 - 0,1 = 50 (g)
C%NaOH = 4/50 = 8%
ĐỀ hỏi nồng độ mol hay nồng độ chất tan vậy, nếu hỏi nồng độ chất tan thì đề lỗi

\(a,C\%_{NaCl}=\dfrac{15}{15+185}.100\%=7,5\%\\ b,m_{HNO_3}=\dfrac{18,9}{100}.100+\dfrac{6,3}{100}.200=31,5\left(g\right)\\ m_{ddHNO_3}=100+200=300\left(g\right)\\ C\%_{HNO_3}=\dfrac{31,5}{300}.100\%=10,5\%\)
\(c,n_{NaCl}=\dfrac{5,85}{58,5}=0,1\left(mol\right)\\ C_{M\left(NaCl\right)}=\dfrac{0,1}{0,1}=1M\\ d,n_{KOH}=2.0,2+0,2.0,2=0,44\left(mol\right)\\ V_{ddKOH}=0,2+0,2=0,4\left(l\right)\\ C_{M\left(KOH\right)}=\dfrac{0,44}{0,4}=1,1M\\ e,m_{NaOH}=\dfrac{150.16}{100}=24\left(g\right)\\ m_{ddNaOH}=50+150=200\left(g\right)\\ C\%_{NaOH}=\dfrac{24}{200}.100\%=12\%\)

a, \(n_{Na_2O}=\dfrac{12,4}{62}=0,2\left(mol\right)\)
PTHH: Na2O + H2O ---> 2NaOH
0,2------------------>0,4
\(\Rightarrow C\%_{NaOH}=\dfrac{0,4.40}{12,4+50}.100\%=25,64\%\)
b, \(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
PTHH: 2Na + 2H2O ---> 2NaOH + H2
0,2------------------->0,2------->0,1
\(\Rightarrow C\%_{NaOH}=\dfrac{0,2.40+16}{100+16+4,6-0,1.2}.100\%==20\%\)
c, \(n_{Na}=\dfrac{9,2}{23}=0,4\left(mol\right)\)
\(n_{HCl}=\dfrac{100.7,3\%}{36,5}=0,2\left(mol\right)\)
PTHH:
2Na + 2HCl ---> 2NaCl + H2
0,2<-----0,2-----------0,2--->0,1
2Na + 2H2O ---> 2NaOH + H2
0,2------------------>0,2----->0,1
\(\Rightarrow m_{dd}=9,2+100-\left(0,1+0,1\right).2=108,8\left(g\right)\\ \Rightarrow\left\{{}\begin{matrix}C\%_{NaCl}=\dfrac{0,2.58,5}{108,8}.100\%=10,75\%\\C\%_{NaOH}=\dfrac{0,2.40}{108,8}.100\%=7,35\%\end{matrix}\right.\)

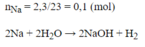
\(n_{Na}=\dfrac{23}{23}=1\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
1------------------->1---->0,5
=> mNaOH = 1.40 = 40 (g)
mdd sau pư = 23 + 100 - 0,5.2 = 122 (g)
=> \(C\%=\dfrac{40}{122}.100\%=32,787\%\)