Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Ta có phản ứng: 2Na + 2H2 → 2NaOH + H2↑.
+ Ta có nNa = 1 mol ⇒ nH2 = 0,5 mol
⇒ mH2 = 0,5×2 = 1 gam.
⇒ mDung dịch sau phản ứng = 23 + 100 – 1 = 122 gam.
+ Ta có nNaOH = 1 mol ⇒ mNaOH = 40 gam.
⇒ C%NaOH = 40 122 × 100 ≈ 32,8%

nNa=1,5mol
nH2O=89/9 mol
ta có PT: 2Na+2H2O=>2NaOH+H2
1,5 : 89/9
ta thấy nH2O dư theo n Na
P/ư: 1,5->1,5 ->1,5->1,5
ta có mNaOH thu được :1,5.40=60g
theo đl btoan klg ta có mddNaOH= mNa+mH2O-mH2
= 34,5+177-1,5.2=208,5g
=> nồng độ phần trăm NaOH: C%=60/208,9.100=18,78%
- Bn ơi mdd của NaOH = 208,5 mà ở dưới tính C% thì bn ghi là 208,9 nên ra kết quả sai r kết quả là C% = 60*100/208.5=28.77 (%) mới đúng.

Khối lượng dung dịch = 108,2 + 3,9 - 0,1 = 112 gam
Khối lượng chất tan = 0,1 x 56 = 5,6 gam
Nồng độ % = 5,6/112 = 0,05 = 5/100 = 5%

Ta có thể viết 2 phản ứng:
Fe+6HNO3 ⇒ Fe(NO3)3 +3NO2 +3H2O
Cu+4HNO3 ⇒ Cu(NO3)2 +2NO2 +2H2O
Có
![]()
Quan sát các phản ứng nhận thấy:
![]()
![]()
Dung dịch A thu được chứa Fe(NO3)3 và Cu(NO3)2.
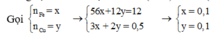
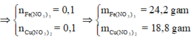
Áp dụng định luật bảo toàn khối lượng ta có:
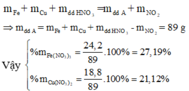
Đáp án B.


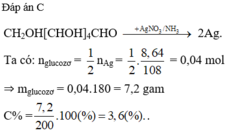
Giải thích:
nNa = 23: 23 = 1 (mol)
2Na + 2H2O → 2NaOH + H2↑
1 →1 → 0,5
mdd sau = mNa + mH2O – mH2 = 23 + 100- 0,5.2 = 122g
Đáp án C