Cho 3,65g đ HCl ( đặc ) tác dụng với MnO2 thu được V ( lít ) khí Clo ( đktc ). Viết PTHH. Tính giá trị của V?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{MnO_2}=\dfrac{17,4}{87}=0,2\left(mol\right)\\ PTHH:MnO_2+4HCl_{đặc,nóng}\rightarrow MnCl_2+Cl_2+2H_2O\\ n_{Cl_2\left(TT\right)}=\dfrac{3,584}{22,4}=0,16\left(mol\right)\\ n_{Cl_2\left(LT\right)}=n_{MnO_2}=0,2\left(mol\right)\\ \Rightarrow H=\dfrac{n_{Cl_2\left(TT\right)}}{n_{Cl_2\left(LT\right)}}.100\%=\dfrac{0,16}{0,2}.100=80\%\)

PTHH: \(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{MnO_2}=\dfrac{17,4}{87}=0,2\left(mol\right)\\n_{HCl}=0,5\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,5}{4}\) \(\Rightarrow\) MnO2 còn dư, tính theo HCl
\(\Rightarrow n_{Cl_2}=0,125\left(mol\right)\) \(\Rightarrow V_{Cl_2}=0,125\cdot22,4=2,8\left(l\right)\)
Cho 150g dd hcl 36,5% tác dụng vs mno2 dư Viết pthh của pháp ứng Tính thể tích khí clo thu được đktc

\(n_{HCl}=\dfrac{150.36,5\%}{36,5}=1,5\left(mol\right)\)
PTHH: MnO2 + 4HCl --> MnCl2 + Cl2 + 2H2O
1,5------------->0,375
=> VCl2 = 0,375.22,4 = 8,4 (l)

- PT: a, \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\) (1)
\(MnO_2+4HCl_đ\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O\) (2)
- Ta có: \(n_{HCl\left(1\right)}=n_{HCl\left(2\right)}=0,2.2=0,4\left(mol\right)\)
Theo PT (1): \(n_{Cl_2}=\dfrac{5}{16}n_{HCl\left(1\right)}=0,125\left(mol\right)\Rightarrow V_1=0,125.22,4=2,8\left(l\right)\)
(2): \(n_{Cl_2\left(2\right)}=\dfrac{1}{4}n_{HCl\left(2\right)}=0,1\left(mol\right)\Rightarrow V_2=0,1.22,4=2,24\left(l\right)\)

Đáp án C
![]()
MnO2 + 4HCl →MnCl2 + 2H2O + Cl2
0,1 →0,1 (mol)
Do H% = 85% => ![]() = 0,085 (mol)
= 0,085 (mol)
V = 0,085.22,4 = 1,904 (lít)

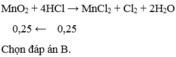

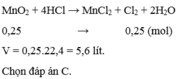
Anh nghĩ 3.65 (g) là khối lượng của HCl luôn ấy em
\(n_{HCl}=\dfrac{3.65}{36.5}=0.1\left(mol\right)\)
\(MnO_2+4HCl_{\left(đ\right)}\rightarrow MnCl_2+Cl_2+2H_2O\)
\(............0.1.............0.025\)
\(V_{Cl_2}=0.025\cdot22.4=0.56\left(l\right)\)
*Chắc là 3,65 gam HCl
PTHH: \(MnO_2+4HCl\rightarrow MnCl_2+Cl_2\uparrow+H_2O\)
Theo PTHH: \(n_{Cl_2}=\dfrac{1}{4}n_{HCl}=\dfrac{1}{4}\cdot\dfrac{3,65}{36,5}=0,025\left(mol\right)\)
\(\Rightarrow V_{Cl_2}=0,025\cdot22,4=0,56\left(l\right)\)