Hòa tan hết 18,4g hỗn hợp Fe và FeO cần dung vừa đủ 300g dung dịch HCl, thu được dung dịch dịch X và 4,48 lít khí thoát ra ở (ĐKC)
a. Viết phương trình hóa học .
b. Tính phần trăm khối lượng của Fe trong hỗn hợp trên .
c. Tính C% muối trong dung dịch X .
( Cho Fe = 56, O = 16, S= 32, H= 1, Cl = 35,5 , N = 14, C = 12)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, Ta có: 27nAl + 56nFe = 22 (1)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{19,832}{24,79}=0,8\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,4\left(mol\right)\\n_{Fe}=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,4.27}{22}.100\%\approx49,09\%\\\%m_{Fe}\approx50,91\%\end{matrix}\right.\)
b, \(n_{HCl}=2n_{H_2}=1,6\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{1,6}{0,5}=3,2\left(M\right)\)

a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c, \(n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\Rightarrow m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
d, \(n_{HCl}=2n_{Zn}=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(\Rightarrow m_{ddHCl}=\dfrac{14,6}{7,3\%}=200\left(g\right)\)
⇒ m dd sau pư = 13 + 200 - 0,2.2 = 212,6 (g)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{27,2}{212,6}.100\%\approx12,79\%\)

Gọi x,y,z lần lượt là số mol của Al,Mg,Zn
PT:
2Al + 6HCl--->2AlCl3 + 3H2
x-------3x----------------------1,5x mol
Mg + 2HCl--->MgCl2 + H2
y-----2y----------------------y mol
Zn + 2HCl--->ZnCl2 + H2
z----2z--------------------z mol
b.
Số mol H2: nH2=16,352/22,4=0,73 mol
1,5x+y+z=0,73
27x = 24y =>x=8y/9
=>7y/3 +z =0,73 (*)
27x + 24y + 65z=19,6
27x = 24y
=> 48y + 65z =19,6 (**)
Từ (*),(**)
=>y=0,27 => mMg =6,48 g
z=0,1=>mZn = 6,5 g
x=0,24=>mAl =6,48g
c.
nHCl =2nH2
=>nHCl =2.0,73=1,46 mol
=>V dd=1,46/2=0,73(l)

Gọi \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo pt: \(\Rightarrow\left\{{}\begin{matrix}3x+y=0,2\\27x+56y=5,5\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{19}{470}\\y=\dfrac{37}{470}\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{\dfrac{19}{470}\cdot27}{5,5}\cdot100\%=19,84\%\)
\(\%m_{Fe}=100\%-19,84\%=80,16\%\)

a, Ta có: 27nAl + 56nFe = 27,8 (1)
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{17,353}{24,79}=0,7\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,2\left(mol\right)\\n_{Fe}=0,4\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{27,8}.100\%\approx19,42\%\\\%m_{Fe}\approx80,58\%\end{matrix}\right.\)
b, \(n_{H_2SO_4}=n_{H_2}=0,7\left(mol\right)\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,7}{0,5}=1,4\left(M\right)\)

a) Gọi $n_{Al} =a (mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b = 13(1)$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Fe + 2HCl \to FeCl_2 + H_2$
Theo PTHH : $n_{H_2} = 1,5a + b = \dfrac{6,72}{22,4} = 0,3(2)$
Từ (1)(2) suy ra : $a = \dfrac{1}{15} ; b = 0,2$
$\%m_{Al} = \dfrac{ \dfrac{1}{15}.27}{13}.100\% = 13,8\%$
$\%m_{Fe} = 100\% - 13,8\% = 86,2\%$
b) $n_{HCl} = 2n_{H_2} = 0,3.2 = 0,6(mol)$
$\Rightarrow C_{M_{HCl}} = \dfrac{0,6}{0,15} = 4M$
c) $n_{muối} = m_{kim\ loại} + m_{HCl} - m_{H_2} = 13 + 0,6.36,5 - 0,3.2 = 34,3(gam)$

a) $2Al + 6HCl \to 2AlCl_3 + 3H_2$
b) n Al = 8,1/27 = 0,3(mol)
Theo PTHH :
n H2 = 3/2 n Al = 0,45(mol)
V H2 = 0,45.22,4 = 10,08(lít)
c) n AlCl3 = n Al = 0,3(mol)
m AlCl3 = 0,3.133,5 = 40,05(gam)
d) n HCl = 3n Al = 0,9(mol)
m dd HCl = 0,9.36,5/7,3% = 450(gam)
Sau phản ứng :
m dd = 8,1 + 450 -0,45.2 = 457,2(gam)
C% AlCl3 = 40,05/457,2 .100% = 8,76%

a. PTHH:
\(BaO+2HCl--->BaCl_2+H_2O\left(1\right)\)
\(BaCO_3+2HCl--->BaCl_2+CO_2\uparrow+H_2O\left(2\right)\)
Ta có: \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT(2): \(n_{BaCO_3}=n_{CO_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{BaCO_3}=0,2.197=39,4\left(g\right)\)
\(\Rightarrow\%_{m_{BaCO_3}}=\dfrac{39,4}{54,7}.100\%=72,03\%\)
\(\%_{m_{BaO}}=100\%-72,03\%=27,97\%\)
b. Ta có: \(m_{BaO}=54,7-39,4=15,3\left(g\right)\)
\(\Rightarrow n_{BaO}=\dfrac{15,3}{153}=0,1\left(mol\right)\)
\(\Rightarrow n_A=0,1+0,2=0,3\left(mol\right)\)
Theo PT(1,2): \(n_{HCl}=2.n_A=2.0,3=0,6\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,6.36,5=21,9\left(g\right)\)
Ta có: \(C_{\%_{HCl}}=\dfrac{21,9}{m_{dd_{HCl}}}.100\%=20\%\)
\(\Rightarrow m_{dd_{HCl}}=109,5\left(g\right)\)
\(n_{CO2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
a) Pt : \(BaO+2HCl\rightarrow BaCl_2+H_2O|\)
1 2 1 1
0,1 0,2
\(BaCO_3+2HCl\rightarrow BaCl_2+CO_2+H_2O|\)
1 2 1 1 1
0,2 0,4 0,2
\(n_{BaCO3}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(m_{BaCO3}=0,2.197=39,4\left(g\right)\)
\(m_{BaO}=54,7-39,4=15,3\left(g\right)\)
0/0BaO = \(\dfrac{15,3.100}{54,7}=27,97\)0/0
0/0BaCO3 = \(\dfrac{39,4.100}{54,7}=72,03\)0/0
b) Có : \(m_{BaO}=15,3\left(g\right)\)
\(n_{BaO}=\dfrac{15,3}{153}=0,1\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,2+0,4=0,6\left(mol\right)\)
\(m_{HCl}=0,6.36,5=21,9\left(g\right)\)
\(m_{ddHCl}=\dfrac{21,9.100}{20}=109,5\left(g\right)\)
Chúc bạn học tốt
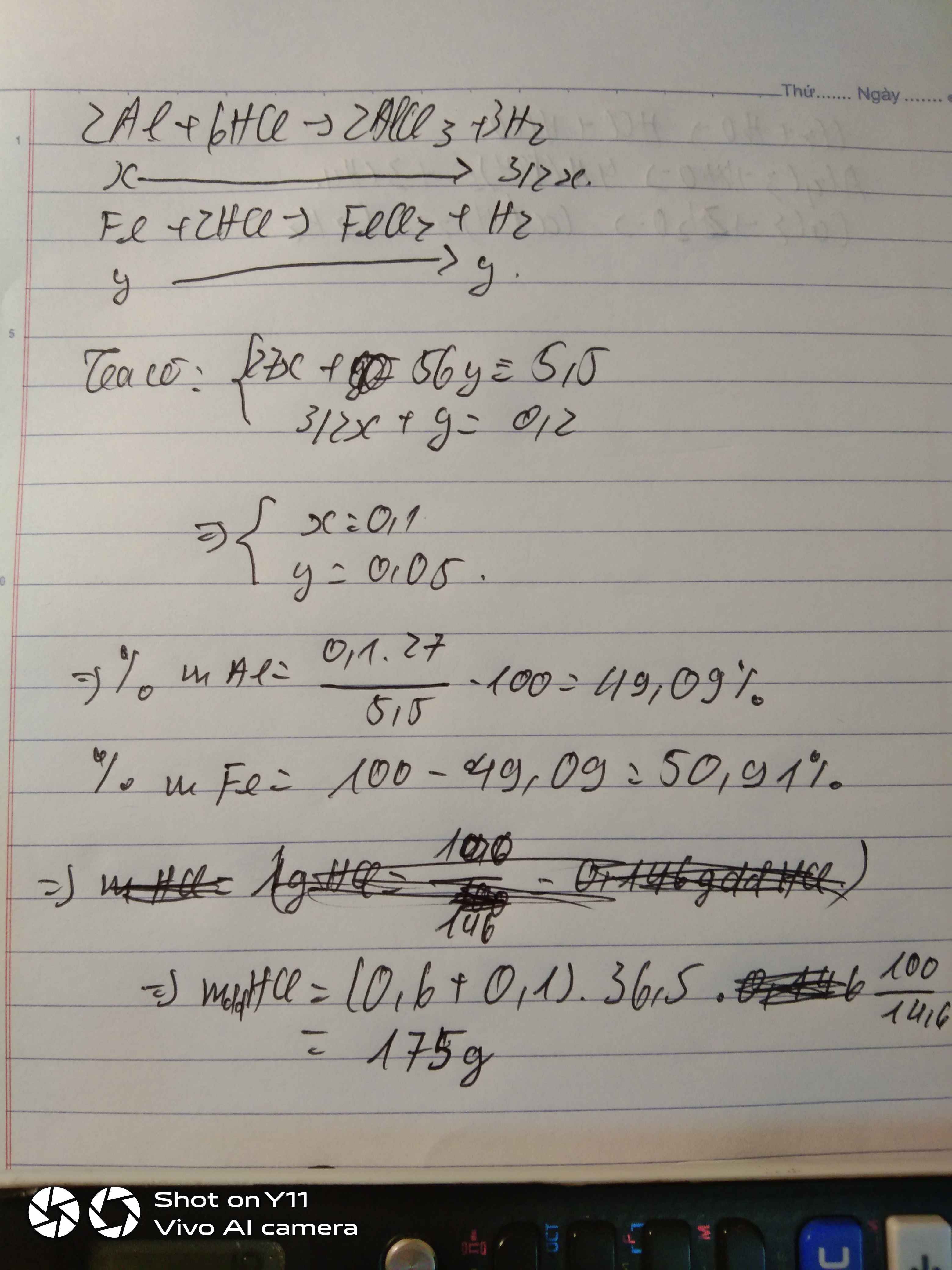
a.Fe + 2HCl -> FeCl2 + H2
0.2 0.4 0.2 0.2
FeO + 2HCl -> FeCl2 + H2O
0.1 0.2 0.1
b.nH2 = 0.2 mol
mFe = \(0.2\times56=11.2g\) => \(\%mFe=\dfrac{11.2\times100}{18.4}=60.9\%\)
c.mFeO = 18.4 - 11.2 = 7.2g => nFeO = 0.1mol
mdd sau phản ứng: mFe + mFeO + mHCl - mH2
= 18.4 + 300 - 0.2\(\times2=318g\)
\(C\%FeCl2=\dfrac{0.3\times127\times100}{318}=11.98\%\)