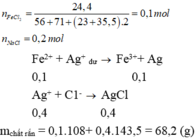Hòa tan hoàn toàn m gam Al vào dd HNO3 dư, sau khi các pư xảy ra hoàn toàn thu dd Y và 985,6 ml N2 (đktc). Sau phản ứng thu được 44,2 gam muối. Giá trị của m là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án : A
Ba + 2H2O -> Ba(OH)2 + H2
Ba(OH)2 + 2Al + H2O -> Ba(AlO2)2 + 3H2
=> nH2 = 4nBa = 0,4 mol => nBa = 0,1 mol
Vì X +NaOH tạo nH2 = 0,7 mol > 0,4 mol => chứng tỏ Al dư ở thí nghiệm đầu
=> nH2 do Al = nH2 (2) – nH2(1) = 0,3 mol
=> nAl = 2/3 nh2 do Al = 0,2 mol
=> mX = 19,1g

\(\left\{{}\begin{matrix}64.n_{Cu}+56.n_{Fe}=8,8\\\dfrac{n_{Cu}}{n_{Fe}}=\dfrac{1}{2}\end{matrix}\right.=>\left\{{}\begin{matrix}n_{Cu}=0,05\\n_{Fe}=0,1\end{matrix}\right.\)
nAgNO3 = 0,3.1,5 = 0,45(mol)
PTHH: Fe + 2AgNO3 --> Fe(NO3)2 + 2Ag\(\downarrow\)
_____0,1--->0,2---------->0,1---------->0,2
Cu + 2AgNO3 --> Cu(NO3)2 + 2Ag\(\downarrow\)
0,05->0,1------------>0,05----->0,1
Fe(NO3)2 + AgNO3 --> Fe(NO3)3 + Ag\(\downarrow\)
___0,1----->0,1---------->0,1--------->0,1
=> nAg = 0,2 + 0,1 + 0,1 = 0,4 (mol)
=> mAg = 0,4.108 = 43,2 (g)

bn tính giùm mk m gam ag đk? tại mk tính ra ko thấy giống...
A. 43,2 gam B. 32,4 gam C. 35,6 gam D. 35,2 gam

Gọi $n_{Na} = a(mol)$
2Na + 2H2O → 2NaOH + H2
a...........................a..........0,5a.....(mol)
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
..a...........a............................................1,5a....(mol)
Suy ra : $0,5a + 1,5a = \dfrac{3,36}{22,4} = 0,15 \Rightarrow a = 0,075$
Vậy :
$m = 0,075.23 + 0,075.27 + 1,35 = 5,1(gam)$
Gọi nNa=a(mol)���=�(���)
2Na + 2H2O → 2NaOH + H2
a...........................a..........0,5a.....(mol)
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
..a...........a............................................1,5a....(mol)
Suy ra : 0,5a+1,5a=3,3622,4=0,15⇒a=0,0750,5�+1,5�=3,3622,4=0,15⇒�=0,075
Vậy :
m=0,075.23+0,075.27+1,35=5,1(gam)