Trong bình kín chứa 11,2l SO2 và 4,48l O2. Châm lửa để phản ứng diễn ra hoàn toàn
Theo PTHH:
2SO2 + O2 -> 2SO3
Tính thể tích khí có trong bình sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ n_{O_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ 2H_2 + O_2 \xrightarrow{t^o} 2H_2O\)
Ta thấy :
\(\dfrac{n_{H_2}}{2} = 0,15 > \dfrac{n_{O_2}}{1} = 0,1\) nên H2 dư
Theo PTHH : \(n_{H_2O} = 2n_{O_2} = 0,2(mol) \Rightarrow m_{H_2O} = 0,2.18 = 3,6(gam)\)
b)
Ta có : \(n_{H_2\ pư} = 2n_{O_2} = 0,2(mol)\\ \Rightarrow n_{H_2\ dư} = 0,3 - 0,2 = 0,1(mol)\\ \Rightarrow V_{H_2\ dư} = 0,1.22,4 = 2,24(lít)\)

Đáp án A
Chọn 100 mol không khí.
Tỉ lệ thể tích cũng là tỉ lệ số mol nên
![]()
Gọi 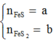
Có
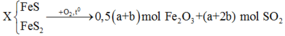

![]()
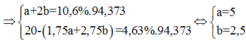

Đáp án : B
Xét 1 mol không khí : 0,2 mol O2 và 0,8 mol N2
%nN2 = 84,77% => nY = 0,94373 mol
=> nSO2 = 0,1 mol
,nO2 dư = 0,0437 mol
=> nO2 pứ = 0,2 – 0,044 = 0,1563 mol
2FeS + 3,5O2 -> Fe2O3 + 2SO2
.a -> 1,75a
2FeS2 + 5,5O2 -> Fe2O3 + 4SO2
.b -> 2,75b
=> ¼ (7a + 11b) = 0,1563
.a + 2b = 0,1
=> a = 0,05 mol ; b = 0,025 mol
=> mX = 7,4g
=> %mFeS = 59,46%

\(n_S=\dfrac{m_S}{M_S}=\dfrac{3,2}{32}=0,1mol\)
\(n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{1,68}{22,4}=0,075mol\)
\(S+O_2\rightarrow\left(t^o\right)SO_2\)
0,1> 0,075 ( mol )
0,075 0,075 ( mol )
\(V_{SO_2}=V_{O_2}=1,68l\)
nSO2= 0,5(mol)
nO2=0,2(mol)
PTHH: 2 SO2 + O2 -to-> 2 SO3
Ta có: 0,5/2 > 0,2/1
=> O2 hết, SO2 dư, tính theo nO2
-> nSO3=nO2.2=0,2.2=0,4(mol)
nSO2(dư)= 0,5-0,2.2=0,1(mol)
=>V(sau p.ứ)= V(SO2,dư,đktc)+V(SO3,đktc)=0,1.22,4+0,4.22,4=11,2(l)