Dung dịch X gồm Ba(OH)2 và Ba(AlO2)2. Nhỏ từ từ dung dịch H2SO4 1M vào dung dịch X thu được kết tủa được biểu diễn bằng đồ thị dưới đây:
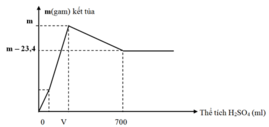
Giá trị m gần nhất với giá trị nào dưới đây ?
A. 88
B. 84
C. 86
D. 82
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Đồ thị trải qua các giai đoạn:
+Kết tủa tăng vừa do Ba(OH)2 tác dụng với H2SO4 tạo BaSO4.
+Kết tủa tăng nhanh do H2SO4 tác dụng với Ba(AlO2)2 tạo 2 kết tủa BaSO4 và Al(OH)3.
+Kết tủa giảm tới không đổi do H2SO4 hòa tan Al(OH)3.
Nhận thấy khối lượng kết tủa lúc cực đại với lúc không đổi giảm 23,4 gam chính là khối lượng Al(OH)3 bị hòa tan.
→ n A l ( O H ) 3 = 0 , 3 m o l
Tới lúc hòa tan kết tủa hoàn toàn thì cần 0,7 mol H2SO4.
Vậy lúc kết tủa cực đại thì chỉ cần 0 , 7 - 0 , 3 . 3 2 = 0 , 25 m o l
Kết tủa cực đại gồm 0,25 mol BaSO4 và 0,3 mol Al(OH)3.
Vậy m=81,65 gam

Chọn đáp án C.
Vì cho thể tích X bao nhiêu thì tỉ lệ nBa(OH)2 : nNaOH = 1:2 nên ta cố định tỉ lệ này với các giai đoạn phản ứng, đặt nH2SO4 ban đầu = a và Al2(SO4)3 ban đầu = b ta có:
Đoạn 1 (chỉ có BaSO4 tạo thành):
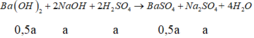
Đoạn 2 (có cả BaSO4 và Al(OH)3):
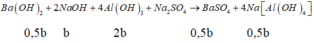
Đoạn 4 (chỉ có BaSO4 tạo thành
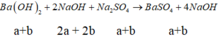
Tại vị trí số mol kết tủa là 0,09 chính là ngay khi kết thúc giai đoạn 2 → 0,5a + 3,5b = 0,09
Tại vị trí thể tích X là 60 ml chính là ngay khi kết thúc giai đoạn 3 → 0,5a + 1,5b + 0,5b = 0,06
Từ đó tính được a = 0,04 và b = 0,02
Tại vị trí thể tích X là x ml chính là giữa chừng của giai đoạn 2
nKết tủa = 0,04 → 0,5a + (x/1000 – 0,5a)×7/3 =0,04 thay a = 0,04 vào = x = 200/7 = 28,571.

Chọn đáp án C.
Vì cho thể tích X bao nhiêu thì tỉ lệ nBa(OH)2 : nNaOH = 1:2 nên ta cố định tỉ lệ này với các giai đoạn phản ứng, đặt nH2SO4 ban đầu = a và Al2(SO4)3 ban đầu = b ta có:
Đoạn 1 (chỉ có BaSO4 tạo thành):
Ba(OH)2 + 2NaOH + 2H2SO4 → BaSO4 + Na2SO4 + 4H2O
0,5а а а 0,5а а
Đoạn 2 (có cả BaSO4 và Al(OH)3):
3Ba(OH)2 + 6NaOH + 2Al2(SO4)3→ 3BaSO4 + 4Al(OH)3 + 3Na2SO4
1,5b 3b b 1,5b 2b 1,5b
Đoạn 3 (Al(OH)3 tan nhiều hơn BaSO4 hình thành):
Ba(OH)2 + 2NaOH + 4Al(OH)3 + Na2SO4 → BaSO4 + 4Na[Al(OH)4]
0,5b b 2b 0,5b 0,5b
Đoạn 4 (chỉ có BaSO4 tạo thành):
Ba(OH)2 + 2NaOH + Na2SO4 → BaSO4 + 4NaOH
a+b 2a + 2b a+b a+b
Tại vị trí số mol kết tủa là 0,09 chính là ngay khi kết thúc giai đoạn 2 → 0,5a + 3,5b = 0,09
Tại vị trí thể tích X là 60 ml chính là ngay khi kết thúc giai đoạn 3 → 0,5a + 1,5b + 0,5b = 0,06
Từ đó tính được a = 0,04 và b = 0,02
Tại vị trí thể tích X là x ml chính là giữa chừng của giai đoạn 2
nKết tủa = 0,04 → 0,5a + (x/1000 – 0,5a)×7/3 =0,04 thay a = 0,04 vào = x = 200/7 = 28,571.

Đáp án C
Hòa tan hoàn toàn m gam X thu được dung dịch Y và 0,45 mol H2.
Do đồ thị như vậy nên giai đoạn đầu kết tủa tăng là do H2SO4 tác dụng với Ba(OH)2 tạo kết tủa BaSO4.
Giai đoạn kết tủa không đổi tiếp theo là H2SO4 trung hòa NaOH.
Giai đoạn kết tủa tăng lên do H2SO4 tác dụng với NaAlO2 tạo kết tủa Al(OH)3.
Giai đoạn kết tủa giảm do H2SO4 hòa tan Al(OH)3.
Giai đoạn kết tủa không đổi lúc này chỉ còn BaSO4
→ 2 n B a ( O H ) 2 + n N a O H = 0 , 4 . 2 = 0 , 8
Kết tủa tối đa là 89,45 gam gồm Al(OH)3 và BaSO4.
Lúc đạt 0,75 mol H2SO4 kết tủa bị giảm đi 7,8 gam tương đương với 0,1 mol Al(OH)3.
Lúc này lượng H2SO4 cần để hòa tan là 0,15 mol.
Vậy lúc kết tủa đạt cực đại thì lượng H2SO4 đã dùng là 0,6 mol
Trong giai đoạn tạo kết tủa Al(OH)3 đã sử dụng 0,2 mol H2SO4
n A l ( O H ) 3 = 0 , 4 m o l → n B a C O 3 = 0 , 25 = n B a ( O H ) 2 → n N a O H = 0 , 3 m o l
Bảo toàn nguyên tố trong X chứa 0,25 mol Ba, 0,4 mol Al và 0,7 mol Na
Bảo toàn e:
n O = 0 , 25 . 2 + 0 , 4 . 3 + 0 , 7 - 0 , 45 . 2 2 = 0 , 75 → m = 73 , 15 g a m

Đáp án C
Hòa tan hoàn toàn m gam X thu được dung dịch Y và 0,45 mol H2.
Do đồ thị như vậy nên giai đoạn đầu kết tủa tăng là do H2SO4 tác dụng với Ba(OH)2 tạo kết tủa BaSO4.
Giai đoạn kết tủa không đổi tiếp theo là H2SO4 trung hòa NaOH.
Giai đoạn kết tủa tăng lên do H2SO4 tác dụng với NaAlO2 tạo kết tủa Al(OH)3.
Giai đoạn kết tủa giảm do H2SO4 hòa tan Al(OH)3.
Giai đoạn kết tủa không đổi lúc này chỉ còn BaSO4
![]()
Kết tủa tối đa là 89,45 gam gồm Al(OH)3 và BaSO4.
Lúc đạt 0,75 mol H2SO4 kết tủa bị giảm đi 7,8 gam tương đương với 0,1 mol Al(OH)3.
Lúc này lượng H2SO4 cần để hòa tan là 0,15 mol.
Vậy lúc kết tủa đạt cực đại thì lượng H2SO4 đã dùng là 0,6 mol
Trong giai đoạn tạo kết tủa Al(OH)3 đã sử dụng 0,2 mol H2SO4
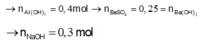
Bảo toàn nguyên tố trong X chứa 0,25 mol Ba, 0,4 mol Al và 0,7 mol Na
Bảo toàn e:

= 0,75
=> m = 73,15 gam
Đáp án D
Đồ thị trải qua các giai đoạn:
+Kết tủa tăng vừa do Ba(OH)2 tác dụng với H2SO4 tạo BaSO4.
+Kết tủa tăng nhanh do H2SO4 tác dụng với Ba(AlO2)2 tạo 2 kết tủa BaSO4 và Al(OH)3.
+Kết tủa giảm tới không đổi do H2SO4 hòa tan Al(OH)3.
Nhận thấy khối lượng kết tủa lúc cực đại với lúc không đổi giảm 23,4 gam chính là khối lượng Al(OH)3 bị hòa tan.
Tới lúc hòa tan kết tủa hoàn toàn thì cần 0,7 mol H2SO4.
Vậy lúc kết tủa cực đại thì chỉ cần 0 , 7 - 0 , 3 . 3 2 = 0 , 25 m o l
Kết tủa cực đại gồm 0,25 mol BaSO4 và 0,3 mol Al(OH)3. Vậy m=81,65 gam